
Cos’è l’enteropatia cronica del gatto? Il termine enteropatia cronica viene utilizzato per descrivere un gruppo di patologie di natura infiammatoria che colpiscono il tratto gastrointestinale del gatto causando sintomi ricorrenti (solitamente di durata superiore ai 21 giorni) di tipologia e gravità variabile. Le enteropatie croniche del gatto vengono ulteriormente classificate in base alla natura della infiammazione intestinale e della risposta a trial terapeutici diversi in: Enteropatia cronica dieto-responsiva Enteropatia cronica responsiva a farmaci immunosoppressivi (anche nota come IBD dall’Inglese inflammatory bowel disease) e Linfoma intestinale a piccole cellule o di basso grado (un tumore di basso grado molto prevalente nel gatto) Quanto comune è l’enteropatia cronica del gatto? Non esistono dati epidemiologici affidabili sulla prevalenza della enteropatia cronica del gatto. Nonostante questo si è assistito a un graduale aumento di casi nell’ultimo decennio per cui la sindrome viene considerata la causa più comune di sintomi gastrointestinali ricorrenti nel gatto adulto. Cosa causa la enteropatia cronica del gatto? La causa esatta della enteropatia cronica del gatto non è nota, tuttavia si sospetta che la patogenesi sia multifattoriale. Ovvero la patologia si instaura per la compresenza e interazione di diversi fattori causali che contribuiscono in maniera più o meno significativa nelle diverse forme di enteropatia cronica. I fattori causali potenzialmente responsabili della enteropatia cronica del gatto includono: Predisposizione genetica Alterazione della flora intestinale (disbiosi) Alterazione del sistema immunitario intestinale (sia la branca acquisita che quella innata) Fattori cosiddetti ambientali tra i quali si annoverano la dieta (sia la quantità che la qualità dei macronutrienti come proteine, grassi, carboidrati e fibra) e farmaci (come antibiotici, anti-infiammatori e gastroprotettori) Esiste una predisposizione di razza, sesso o età nella enteropatia cronica del gatto? Non esiste predisposizione nota di razza, sesso o età nella enteropatia cronica felina. Detto questo, la forma dieto-responsiva della patologia tende a interessare gatti giovani e adulti mentre l’IBD e il linfoma a piccole cellule colpiscono più frequentemente gatti di mezza età o geriatrici. Quali sono i segni clinici tipici della enteropatia cronica del gatto? Il quadro sintomatico di un gatto con enteropatia cronica dipenderà dalla gravità e dallo durata della patologia. I segni clinici più comunemente riportati (in ordine decrescente di frequenza) sono: Perdita di peso corporeo Vomito (di bile o cibo) Diminuzione o perdita completa di appetito (disoressia o anoressia) Diarrea I segni clinici sopracitati non sono specifici della enteropatia cronica felina ma sono comuni ad altri disturbi del tratto digerente del gatto così come patologie del fegato o del pancreas. Pertanto una tale sintomatologia od anche solo il dimagrimento o la scarsa condizione corporea e muscolare devono far preoccupare e spingere a consultare il più presto possibile in proprio veterinario di fiducia, il quale potrebbe dover intraprendere un iter diagnostico volto a identificare la causa dei sintomi e valutare la presenza di patologie concomitanti. Quali sono le indagini da effettuare in un gatto con sospetta enteropatia cronica? Nel caso il gatto presenti sintomi gastrointestinali cronici è necessario un iter diagnostico iniziale volto a escludere altre patologie intestinali possibilmente responsabili dei sintomi (confermando ulteriormente il sospetto di enteropatia cronica), valutare la presenza di patologie concomitanti e identificare la presenza di complicazioni secondarie alla enteropatia cronica. L’iter diagnostico include esami di laboratorio di base (su sangue, urine e feci), esami specifici di funzionalità del pancreas e del piccolo intestino (come il dosaggio delle lipasi pancreatiche sieriche, del TLI sierico e dell’acido folico e della cobalamina sierici) e diagnostica per immagini addominale come l’esame ecografico addominale. Si ricorda che queste indagini non permetteranno di eseguire di una diagnosi definitiva di enteropatia cronica ma di aumentare il sospetto diagnostico della patologia, identificare la presenza di complicazioni della patologia (come ad esempio carenze vitaminiche, anemia cronica, malnutrizione) e valutare la presenza di patologie concomitanti (come malattie infiammatorie di fegato e pancreas, insufficienza renale o ipertiroidismo) in parte responsabili dei sintomi presentati dal gatto. Queste indagini inoltre permetteranno di capire la gravità del quadro clinico e determinare la necessità di iniziare terapie sintomatiche prima di procedere con la diagnosi definitiva. Quali sono le alterazioni ecografiche riscontrabili in corso di enteropatia cronica del gatto? L’esame ecografico addominale è fondamentale nell’approccio diagnostico al gatto con sospetta enteropatia cronica. Questo esame permette valutare lo spessore totale e dei diversi strati della parete intestinale (dall’interno verso l’esterno: mucosa, sottomucosa, muscolare e sierosa) sia dell’intestino tenue che del grosso intestino (Fig.1). Inoltre permette di valutare le dimensioni e architettura degli organi annessi al tratto digerente (fegato, vie biliari e pancreas) così come di valutare forma, dimensioni e architettura dei linfonodi mesenterici (organi linfatici che drenano l’intestino e gli organi addominali). In corso di enteropatia cronica i rilievi dell’esame ecografico dipenderanno dalla gravità e durata della enteropatia e dalla presenza di malattie concomitanti. I rilievi più comuni includono l’ispessimento diffuso (più o meno significativo) della parete intestinale con maggior interessamento dello strato mucosale e muscolare), con o senza perdita della normale stratificazione (Fig. 2), e l’aumento di volume dei linfonodi tributari. E’ importante sottolineare che l’esame ecografico non permette di distinguere tra i vari tipi eziologici di enteropatia del gatto (dieto-responsivo, IBD, linfoma a piccole cellule) in quanto spesso i rilievi ecografici sono sovrapponibili. Inoltre, l’assenza di alterazioni ecografiche non esclude la presenza di enteropatia cronica. Pertanto, l’esame ecografico non va considerato un test diagnostico definitivo ma piuttosto un supporto al sospetto clinico della patologia. Fig. 1 - Immagine ecografica di un ansa intestinale di un gatto sano. Si riconoscono i 4 strati della parete intestinale a partire dall’interfaccia tra l’interno dell’intestino e lo strato della mucosa (linea blu), strato della mucosa (linea gialla), strato della sottomucosa (linea rossa), strato muscolare (linea verde) e strato della sierosa (linea arancione).Fig. 2 - Immagine ecografica di una ansa del piccolo intestino in un gatto affetto enteropatia cronica (precisamente da IBD). Si nota l'aumento lieve dello spessore dello strato muscolare (+1) e dello strato mucosale (+). E’ ancora possibile distinguere uno dall’altro i quattro strati della parete intestinale.E’ possibile avere una diagnosi definitiva di enteropatia cronica del gatto? Il Medico Veterinario potrà voler effettuare una biopsia intestinale poichè il gold standard diagnostico per la diagnosi di enteropatia cronica del gatto e per l’identificazione del tipo causale è l’esame istopatologico su tessuto intestinale. Questo permetterà di valutare la presenza di alterazioni strutturali dei vari strati della parete intestinale in grado di causare i sintomi oltre che la natura, gravità e estensione dell’infiltrato infiammatorio che permetterà di distinguere le forme infiammatorie (enteropatia dieto-responsiva e IBD) da quelle tumorali (linfoma a piccole cellule) di enteropatia cronica. In casi equivoci, dove la distinzione tra forma infiammatoria o tumorale della patologia non è chiara, sarà inoltre possibile effettuare sul tessuto bioptico prelevato delle indagini aggiuntive come l’immunoistochimica o la PARR (un test di biologia molecolare). Come vengono raccolte le biopsie intestinali necessarie per la diagnosi istopatologica di enteropatia cronica del gatto? Vi sono due metodi principali di raccolta delle biopsie intestinali Endoscopia-guidato: consiste nell’utilizzo di uno strumento tubulare flessibile contente una video camera e un canale di lavoro interno che permette di visualizzare l’interno del tratto digerente (tipicamente stomaco, duodeno, ileo e colon) e campionare attraverso una pinza flessibile le aree della mucosa intestinale alterate. I vantaggi di questa metodica consistono nella limitata invasività, nella possibilità di effettuare multiple biopsie con l’ausilio visivo dell’operatore e nella velocità di recupero dalla procedura. I limiti consistono nella ridotta dimensione e superficialità delle biopsie (gli strati) e nella difficoltà di esaminare e campionare tratti del tubo digerente non o difficilmente raggiungibili come il digiuno e l’ileo (spesso interessati dal linfoma a piccole cellule). Chirurgiche (anche dette a tutto spessore): per ottenere le biopsie, il gatto viene sottoposto a una chirurgia esplorativa dell’addome (laparotomia o celiotomia) per poi identificare anse intestinali di interesse ed effettuare delle biopsie cosiddette a tutto spessore che coinvolgono cioè tutti gli strati della parete intestinale. Questo metodo è ovviamente più invasivo e comporta dei rischi post-procedurali anche se rari come la deiscenza della sutura intestinale e l’insorgenza di peritonite settica o infezione della sutura addominale. I vantaggi di questa tecnica riguardano la qualità del tessuto bioptico raccolto (che permette di valutare anche strati più profondi della parete intestinale (non accessibili endoscopicamente) e la possibilità di campionare tratti del piccolo intestino, come il digiuno o l’ileo, non sempre raggiungibili endoscopicamente. Un altro vantaggio di questa metodica è quello di permettere il campionamento in sede di esplorazione chirurgica anche di organi limitrofi come fegato e pancreas (che possono essere coinvolti dal processo patologico intestinale) o dei linfonodi addominali tributari (che permette di valutare l’estensione e la natura della enteropatia cronica). Il Medico Veterinario sceglierà il metodo di campionamento intestinale più consono al caso specifico. Qual è la prognosi dell’enteropatia cronica del gatto? La prognosi dell’enteropatia cronica nel gatto dipenderà dalla tipologia di enteropatia (infiammatoria oppure tumorale), dalla durata e gravità della malattia e delle alterazioni istologiche intestinali e della presenza o meno di complicazioni o malattie concomitanti in grado di influenzare negativamente la qualità di vita del gatto. Generalmente la prognosi con l’enteropatia cronica felina nel lungo termine è buona ma migliore nel caso della enteropatia dieto-responsiva e della IBD rispetto al linfoma alimentare a piccole cellule. Un importante fattore prognostico è rappresentato dall’ottenimento o meno della remissione clinica una volta instaurata la terapia medica.“Med. Vet., Diplomato ACVIM, Diplomato ECVIM-CA, MRCVS, EBVS® - Specialist in Small Animal Internal Medicine”Dr. Fabio ProcoliAutore #sppb-addon-1719818877863 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877863 img{}#sppb-addon-1719818877864 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877864 img{}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}

Cos’è la colecistite acuta? La colecistite è una patologia infiammatoria a carico della colecisti (cistifellea), un piccolo organo muscolare saccato annesso al fegato e deputato alla raccolta della bile che viene poi rilasciata nel piccolo intestino per facilitare la digestione soprattutto dei grassi assunti con l’alimento. Le cause di colecistite nel cane e nel gatto sono molteplici e in base alla durata della malattia la colecistite viene classificata in acuta (rapida insorgenza) o cronica (insorgenza superiore ai 21 giorni).Quali sono le cause di colecistite acuta? La causa più comune di colecistite nel cane e nel gatto è rappresentata da una infezione batterica. Questa può avvenire per invasione delle vie biliari da parte di batteri residenti nel tratto digerente (enterobatteri) o in alternativa può essere causata dalla traslocazione di batteri attraverso il sangue (via ematogena) a partire da un focolaio settico situato in un altro distretto corporeo. Esistono dei fattori predisponenti l’insorgenza di colecistite acuta nel cane e nel gatto? Diversi sono i fattori che possono predisporre all’insorgenza di colecistite sia intrinseci che estrinseci alla cistifellea. Questi includono tumori delle vie biliari, stasi biliare (rallentamento al flusso di bile), formazioni di calcoli in cistifellea (colecistolitiasi) e mucocele biliare (eccessiva formazione e sedimentazione di muco all’interno della cistifellea). Tali condizioni possono creare uno stimolo infiammatorio persistente e indurre la formazione di un ambiente favorevole alla crescita e sopravvivenza batterica. Quali sono i segni clinici di un cane o un gatto affetto da colecistite acuta? Nella fase iniziale, la colecistite può avere un andamento subdolo per cui i nostri animali non manifestano particolari sintomi clinici. Nella fase conclamata della malattia i sintomi più frequentemente riportati nel cane e nel gatto sono: abbattimento/letargia disoressia/anoressia (diminuzione/perdita totale dell’appetito) vomito dolore addominale febbre ittero (colorazione giallastra della cute, delle sclere e delle mucose orali) Come si fa diagnosi di colecistite? Il sospetto di colecistite viene solitamente posto in presenza di sintomi clinici (come quelli precedentemente descritti) ed anche in presenza di alterazioni degli esami ematologici che possono riflettere un disturbo epatobiliare come ad esempio l’aumento degli enzimi epatici (ALT, ALP e GGT) con o senza l’aumento della bilirubina sierica (il pigmento che può dare la colorazione giallastra di cute e mucose ovvero l’ittero). Anche l’esame emocromocitometrico può fornire ulteriori indicazioni di infiammazione acuta o di infezione. Una volta riscontrato il sospetto di una patologia epatobiliare, il metodo diagnostico più utile per supportare ulteriormente la diagnosi di colecistite è l’ecografia addominale. Questa permette di valutare le dimensioni della cistifellea oltre che lo spessore della parete e il suo contenuto. I reperti più comuni in corso di colecistite sono l’ispessimento e l’irregolarità della parete della cistifellea, la presenza di sedimento biliare in sospensione o adeso alla parete, la presenza di calcoli (Fig.1), la reattività dei tessuti e del grasso circostanti oltre che l’aumento di volume dei linfonodi tributari. Talvolta, seppur raramente, per una valutazione più accurata delle vie biliari può essere indicata una diagnostica per immagini di secondo livello come la TAC con mezzo di contrasto. Una volta riscontrata l’alterazione della cistifellea, è possibile confermare la presenza di una causa batterica della colecistite attraverso il prelievo e l’esame citologico e colturale della bile. Studi recenti sia nel cane che nel gatto dimostrano che nel 60% circa dei casi si riscontra la presenza di batteri nella bile. Le specie più comunemente isolate sono tutte di origine intestinale come Escherichia coil, Enteroccoccus Clostridium e Streptococcus. Fig. 1 - Immagine ecografica in un cane con colecistite batterica. Si noti la parete della cistifellea ispessita (*) e la presenza di materiale disomogeneo (**) in sospensione oltre che di un calcolo (***) all’interno della colecistiQuali sono le complicazioni della colecistite acuta? Una delle complicazioni più serie, seppure rara, della colecistite è la rottura della cistifellea con l’insorgenza di una peritonite biliare. La rottura può avvenire in caso di sovradistensione della cistifellea secondaria a ostruzione delle vie biliari extra-epatiche o per la necrosi (degenerazione) della parete della cistifellea (colecistite necrotizzante). La diagnosi di peritonite biliare viene effettuata valutando i sintomi clinici (dolore addominale) e riscontrando ecograficamente segni di perforazione della parete (Fig. 2) quali liquido attorno alla cistifellea, reattività del grasso circostante e presenza di versamento libero in addome. Se campionato il liquido avrebbe il colore giallo-brunastro tipico della bile. La peritonite biliare rappresenta un’emergenza chirurgica per cui sarà necessaria l’asportazione della cistifellea (colecistectomia d’urgenza). Fig. 2 - Colecisti gravemente sovradistesa in un cane con colecistite batterica. Si noti l’ispessimento della parete con aspetto disomogeneo con sospetta perforazione della parete (*). Cos’è la colecistite enfisematosa? La colecistite enfisematosa rappresenta un’altra complicazione della colecistite batterica causata dalla produzione di gas da parte dei batteri. Il gas può accumularsi nello spessore della parete, all’interno dell’organo o nei tessuti circostanti. I segni clinici e gli esami di laboratorio sono sovrapponibili alla colecistite acuta, mentre ecograficamente si riscontra la presenza di un’opacità gassosa all’interno o nella parete della cistifellea. Qual è la prognosi della colecistite acuta nel cane e nel gatto? La prognosi della colecistite acuta dipenderà dalla gravità della patologia e dall’insorgenza delle complicazioni sopracitate. Se tempestivamente identificata e trattata la colecistite può andare in remissione completa. Talvolta saranno necessari monitoraggi seriali nel tempo per verificare che non si sviluppi una colecistite cronica o che non si verifichino complicazioni non presenti al momento della diagnosi. “Med. Vet., Diplomato ACVIM, Diplomato ECVIM-CA, MRCVS, EBVS® - Specialist in Small Animal Internal Medicine”Dr. Fabio ProcoliAutore #sppb-addon-1719818877863 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877863 img{}#sppb-addon-1719818877864 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877864 img{}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}

Luci, colori, festeggiamenti e fuochi artificiali. Questo e molto altro è il nostro modo di festeggiare il nuovo anno che arriva. Questo, però, se per noi è festa può diventare una vera tortura per un cane così come per molti gatti ed altri animali. In molte città accade spesso che il bilancio del primo giorno dell’anno sia tragico per quei cani che vivono all’esterno, nei giardini o in campagna perché moltissimi di loro vivono con terrore la notte di capodanno e i fuochi artificiali che illuminano il cielo ma, soprattutto, producono rumori violentissimi. La fonofobia è un problema diffusissimo nei cani ed è facile immaginare il perché se si considera che il cane ha una grande sensibilità acustica e visiva. La notte di capodanno, trovandosi da solo nel pieno di una super-stimolazione sensoriale, fatta di luci abbaglianti e rumori fortissimi, un cane può avere moltissima paura, fino ad arrivare ad un vero e proprio attacco di panico. I soggetti che soffrono di questo problema, quindi, possono manifestarlo a diversi livelli di gravità. Ci sono cani che hanno semplicemente paura durante i fuochi artificiali e la manifestano cercando il contatto fisico, sobbalzano quando sentono i botti, seguono in casa oppure cercano un rifugio negli angoli più appartati dell’abitazione. Altri cani, invece, tremano, cercano una via di fuga o si muovono incessantemente ansimando, possono addirittura ferirsi graffiando contro le porte o un muro, possono avere scialorrea o attacchi di dissenteria. Infine, ci sono quei soggetti che perdono letteralmente il controllo di sé, in preda ad un vero attacco di panico, quelli che più rischiano la vita, inconsapevoli di ciò che fanno e che rischiano di finire investiti se riescono a scappare o di lanciarsi da una finestra se malauguratamente la trovano aperta. È importantissimo, quindi, prestare attenzione al cane quando si nota che soffre di questa paura, magari palesata durante un temporale o ai primi piccoli botti nei giorni che precedono le feste. Cosa fare per aiutarli? Agire preventivamente può essere letteralmente vitale per l’animale. Per quei cani che solitamente vivono in giardino, sarà necessario trovare una collocazione sicura. Le cronache raccontano di numerosi animali morti investiti nella notte di capodanno, perché stavano vagando disorientati nel traffico e nel frastuono dei festeggiamenti. Questi cani dovrebbero essere abituati già qualche giorno prima ad entrare in casa, così da poterli mettere al sicuro nelle sere centrali delle festività, quando tra le prove e i festeggiamenti si sentiranno gli spari. In questo modo potranno essere collocati in un ambiente sicuro, in casa, scegliendo una stanza quanto più possibile isolata e si eviterà che rischino la vita presi dalla fortissima paura. Per attenuare la paura anche degli animali che vivono all’interno delle nostre abitazioni è possibile fare qualcosa. L’isolamento acustico e visivo è determinante per attenuare il terrore che possono provare questi cani, perciò dovremmo scegliere di adibire per loro una stanza senza finestre, o dove si possano chiudere bene vetri e tapparelle, cercando di creare un ambiente confortevole per loro. Possiamo mettere della musica di sottofondo per attenuare i rumori esterni, questo aiuterà l’animale a ridurre l’iper-vigilanza rispetto a quanto accade all’esterno, predisponendolo meglio ad accogliere il nostro aiuto. Un altro aiuto importante sarà il nostro atteggiamento rispetto al cane e a quanto accade fuori casa. Innanzitutto il cane dovrà sentirsi accolto, fisicamente in casa ma anche rispetto a ciò che prova. Mostrarsi indifferenti o, peggio, sgridarlo non farà che peggiorare le cose. Un cane spaventato, infatti, esattamente come noi, ha bisogno di sentire che può fare conto sulle persone che rappresentano per lui un punto di riferimento. Nel momento della paura avere qualcuno accanto che può aiutarlo è fondamentale. La paura è un’emozione vitale nelle situazioni che mettono in pericolo la vita e un cane che ha paura dei fuochi artificiali si sente in pericolo di vita quando si trova nel mezzo al “bombardamento” della notte di capodanno. Il conforto, l’accoglienza, le attenzioni per attenuare luci e rumori sono il primo passo. Quando cominciano i festeggiamenti, poi, sarà importante l’aiuto attivo. Sarà molto utile porsi con un atteggiamento sereno, tranquillo, allegro, perché questo potrà ispirare tranquillità nel cane, se si fida sufficientemente di noi. Può essere utile proporre un gioco che lo diverte, oppure semplicemente sederci accanto al cane accarezzandolo o semplicemente festeggiare cercando di coinvolgerlo in un clima festoso e distrarlo da ciò che accade fuori dalla casa. Prima e dopo i festeggiamenti. Per evitare di aggravare la paura con ulteriori traumi o, ancora peggio possibili incidenti, sarà necessario scegliere con cura l’orario e le modalità di uscita in passeggiata. È bene evitare le uscite durante le ore clou della sera di festa, scegliendo piuttosto orari tranquilli dove sono minori le possibilità di sentire botti improvvisi. Un'altra importante attenzione è di evitare le uscite in libertà anche per un rapido bisogno, che sia in giardino o al parco. Un botto improvviso potrebbe provocare una forte paura, la fuga, l’aggravamento dello stato di allerta e complicare le ore successive. Prima di uscire di casa è bene accertarsi che il collare o la pettorina siano ben stretti, il guinzaglio andrà tenuto ben saldo tra le mani e nel caso dovessero sentirsi botti all’improvviso potrebbe essere necessario contenere il cane in braccio, se possibile, o direttamente da collare o pettorina ed allontanarsi dal rumore. Prevenire per curare. Per i cani che presentano sintomi seri a causa dei rumori da sparo, come tremori, tachipnea, tachicardia, dissenteria o che abbiano già messo in atto tentativi di fuga in passato, sarebbe opportuno provvedere per tempo ad una visita veterinaria comportamentale. Esistono in commercio molti prodotti naturali che possono dare conforto all’animale che soffre di fonofobia, molti accorgimenti che saranno da individuare sulla base del soggetto, del tipo di abitazione, delle risorse famigliari. Agire per tempo vorrà dire poter vivere le festività con maggior serenità del cane e di tutta la famiglia, riducendo la paura anche degli eventi futuri. “Med. Vet., PhD, Esperto in comportamento animale riconosciuto FNOVI, Presidente SISCA (Società Italiana Scienze Comportamentali Applicate) - (Medicina comportamentale)”Dr.ssa Maria Chiara CatalaniAutore #sppb-addon-1719818877863 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877863 img{}#sppb-addon-1719818877864 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877864 img{}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}

Cos’è la malattia renale cronica del gatto? La malattia renale cronica, anche nota con l’acronimo CKD (dall’Inglese chronic kidney disease) è la patologia più comunemente riscontrata nei gatti di età geriatrica. E’ causata dalla riduzione cronica (più di 3 mesi di durata) e persistente della funzionalità di uno o entrambi i reni. La malattia renale cronica ha un andamento progressivo e irreversibile. Non sempre il grado di perdita di funzionalità è proporzionato all’entità del danno strutturale del rene. Pertanto, è importante l’identificazione precoce della malattia per instaurare una corretta gestione terapeutica e rallentarne la progressione evitando eventuali ripercussioni generali. Cosa causa la malattia renale cronica del gatto? Non sempre è possibile risalire alla causa esatta della malattia renale cronica per cui la malattia viene definita come idiopatica. Tuttavia, diverse sono le possibili cause predisponenti a un danno renale e alla successiva insorgenza di fibrosi e infiammazione interstiziale con conseguente insorgenza di malattia renale cronica. Nel gatto queste includono infezioni batteriche delle vie urinarie alte (pielonefriti), infezioni da virus (come il FIV), ipertensione sistemica, eventi ischemici, assunzione di farmaci nefrotossici o ingestione di tossine, ostruzione delle vie urinarie da calcoli, accumulo di sostanza amiloide (amiloidosi renale), tumori renali ed infine anomalie congenite (come il rene policistico). Nonostante la presenza di una causa sottostante, spesso la diagnosi viene fatta tardivamente quando la malattia è già in uno stadio avanzato ma la causa scatenante non è più presente. Qual è la prevalenza della malattia renale cronica del gatto? Si stima che circa il 30-40% dei gatti di età superiore ai 10 anni sia affetto da malattia renale cronica.Diversi studi scientifici hanno riportato una predisposizione di razza per la malattia con Main Coon, Abissino, Blu di Russia, Burmese e Siamese soggetti a un rischio maggiore di sviluppare la malattia. Quali sono i sintomi tipici della malattia renale cronica del gatto? Negli stadi iniziali della malattia il gatto affetto da malattia renale cronica può essere del tutto asintomatico. Quando presenti i sintomi riportati sono diversi e includono: Aumento della sete e della urinazione (poliuria e polidipsia) Perdita di peso Appetito altalenante Sintomi gastrointestinali intermittenti (nausea, vomito, diarrea) Negli stadi avanzati o terminali ai sintomi sopracitati possono aggiungersi Anoressia (perdita dell’appetito) Letargia Alito uremico Ulcere orali e stomatiti Pallore delle mucose Come faccio sapere se il mio gatto ha la malattia renale cronica? La presenza di malattia renale cronica viene sospettata in presenza di sintomi compatibili in un gatto di età avanzata. Tuttavia, spesso la diagnosi viene fatta accidentalmente in corso di indagini diagnostiche preventive o effettuate prima di una anestesia generale o procedura elettiva (come ad esempio pulizia o estrazione dentali). Perchè sono importanti gli esami di laboratorio per la diagnosi di malattia renale cronica del gatto? La diagnosi di malattia renale cronica viene tipicamente emessa dopo aver riscontrato i segni di insufficienza renale negli esami di laboratorio su sangue ed urine. Le alterazioni di laboratorio indicative di insufficienza renale sono: Aumento dell'urea e creatinina sieriche Aumento della SDMA (che può insorgere anche con urea e creatinina normale) Urine poco concentrate (peso specifico urinario inferiore a 1.035) in associazione al rialzo della creatinina e/o SDMA. Inoltre le analisi di laboratorio possono mostrare anche alterazioni che insorgono come conseguenza dalla malattia renale stessa. Per gli esami ematici queste includono: Acidemia (riduzione del pH del sangue) Aumento del fosforo Diminuzione o aumento del calcio Diminuzione del potassio Anemia lieve-moderata non rigenerativa Per l’esame delle urine le alterazioni aggiuntive includono: Presenza o meno cellule infiammatorie o batteri Presenza di cilindri Accumulo di proteine (proteinuria) Perchè è importante l’esame ecografico in corso di malattia renale cronica? L'esame ecografico può rilevare alterazioni nella architettura di uno o entrambi i reni anche in assenza di alterazioni degli esami ematologici.I reni in corso di malattia renale cronica tendono a perdere la normale architettura. Uno dei primi segni di malattia renale cronica è la perdita della netta distinzione tra la corticale (regione più esterna) e la midollare (regione più interna) del rene solitamente facilmente distinguibili per via ecografica. (Fig. 1) In aggiunta le dimensioni dei reni possono ridursi e possono comparire alterazioni nella loro forma o mineralizzazioni del parenchima ed inoltre potrebbero essere visibile i segni della causa della malattia renale come la pielonefrite (con dilatazione dei bacinetti renali e reattività del grasso e presenza di liquido libero circostante i reni), la presenza di calcoli nei bacinetti renali, negli ureteri o in vescica o la presenza di cisti multiple (rene policistico) o neoformazioni indicative di tumori. Quanti stadi esistono di malattia renale cronica del gatto? Fondamentalmente esistono 4 stadi di gravità (in ordine crescente dall’1 al 4) così definiti dalla Società Internazionale di Interesse Renale (IRIS). Lo stadio viene determinato in base ai valori della creatinina sierica e della SDMA. Per ogni stadio esistono dei sottostadi determinati dalla presenza o meno di marker prognostici come l’aumento del fosforo ematico, l’accumulo di proteine nelle urine e l’ipertensione arteriosa. Ad ogni stadio corrisponde la probabilità o meno di presentare dei sintomi clinici e sviluppare complicazioni sistemiche oltre che una prognosi più o meno favorevole nel lungo termine. Quali sono le complicazioni della malattia renale cronica? La malattia renale cronica nel tempo può portare all’insorgenza di una serie di complicazioni anche al di fuori dell’apparato urinario che possono impattare negativamente la qualità di vita e la prognosi del gatto. Le complicazioni meglio descritte della malattia renale cronica nel gatto sono: l'anemia cronica non rigenerativa secondaria alla ridotta produzione dell’ormone “eritropoietina” dal rene malato (ormone responsabile della produzione di globuli rossi da parte del midollo osseo). L’anemia se molto grave può peggiorare la qualità di vita del gatto o comprometterne la sua sopravvivenza;l’alterazione dei meccanismi di escrezione e riassorbimento di sostanze tamponanti da parte del rene può portare alla eccessiva acidificazione del sangue (acidosi metabolica); un’altra conseguenza della malattia renale molto frequente è la comparsa di ipertensione arteriosa, che se grave e non trattata può provocare danni vascolari ai piccoli capillari di organi target come cervello, cuore e occhio. Fig.1 - Ecografia di un gatto con malattia renale cronica avanzata. Si noti la perdita della normale distinzione cortico-midollare (parentesi), l’aspetto irregolare del profilo renale e il lieve versamento perirenale (freccia).Qual è la prognosi della malattia renale cronica del gatto e perchè è importate la medicina preventiva ? La prognosi di un gatto con malattia renale cronica dipende fondamentalmente dallo stadio della malattia (peggiora all’aumentare dello stadio di gravità) e dalla comparsa di complicazioni secondarie alcune potenzialmente fatali se non riconosciute e gestite. Fondamentali saranno ai fini prognostici la tempestiva identificazione della malattia renale e delle sue complicazioni e la loro gestione terapeutica. In generale, la malattia renale cronica rappresenta la causa di morte in circa il 13% dei gatti di età superiore ai 15 anni ma se tenuta sotto controllo consente una buona qualità di vita anche nel lungo termine. Per questo motivo è importante chiedere al proprio veterinario di fiducia di eseguire check up preventivi periodici in modo da poter escludere o diagnosticare precocemente la malattia renale cronica del proprio gatto.“Med. Vet., Diplomato ACVIM, Diplomato ECVIM-CA, MRCVS, EBVS® - Specialist in Small Animal Internal Medicine”Dr. Fabio ProcoliAutore #sppb-addon-1719818877863 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877863 img{}#sppb-addon-1719818877864 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877864 img{}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}

I seni paranali o sacchi anali, presenti sia nel cane sia nel gatto, sono due “sacchettini” localizzati alle ore “4” e “8” della regione anale, circondati da fibre del muscolo sfintere esterno dell’ano. Le loro pareti sono tappezzate da ghiandole apocrine e il loro secreto, maleodorante per gli umani, è evacuato attraverso un dotto (in cui sono presenti anche ghiandole sebacee) localizzato a livello della giunzione mucocutanea, tra gli sfinteri esterno e interno dell’ano. Le patologie più comuni sono l’intasamento, la sacculite (a volte accompagnata da fistolizzazione esterna) ed i tumori. Tra i tumori, il più importante è l’adenocarcinoma apocrino, più raro il melanoma ed altri tipi di neoplasie. I cani colpiti sono più spesso di media taglia, senza predisposizione di sesso. L’adenocarcinoma del seno paranale è molto raro nel gatto. Quali i possibili segni clinici che conducono a visita? Può innanzi tutto essere che il tumore ai lati dell’ano passi inosservato (nel 40% dei casi) per qualche tempo perché di piccole dimensioni e venga svelato solo durante un’esplorazione digitorettale eseguita per altre ragioni. Per questo motivo è sempre bene far visitare periodicamente il proprio cane dal Veterinario di fiducia anche se non manifesta alcun sintomo clinico. In altri casi, invece, il paziente manifesta difficoltà nella defecazione, per la grandezza della massa o, molto più spesso, per ingrandimento metastatico dei linfonodi della regione (sotto alla colonna vertebrale e al di sopra dell’ultimo tratto dell’intestino, il coloretto) e/o aumento della sete e della quantità di urina prodotta. L’aumento della sete e della produzione urinaria è indotto da un aumento del calcio nel sangue (ipercalcemia) a causa di una sostanza prodotta dal tumore, sia dal tumore primario sia dalle sue eventuali metastasi (nei linfonodi regionali o in altre sedi lontane – fegato, milza, polmoni, linfonodi di altre sedi, osso, etc.). Diagnosi ed esami collaterali La diagnosi si basa sulla visita clinica con esplorazione digito-rettale e su ulteriori esami che il veterinario potrà richiedere come ad esempio: ago-aspirato ed esame citologico del tumore primario, esame ecografico dell’addome e radiografico del torace oltre ad esami del sangue. Al fine, però, di programmare l’intervento chirurgico il veterinario potrà richiedere un esame TC completo “total body”. Se è presente ipercalcemia, riscontrata con gli esami ematologici, il veterinario prescriverà una terapia adeguata perché può provocare danni renali. Paziente chirurgico è quello che, dopo tutti gli accertamenti, mostra solo il tumore primario, o il tumore primario in regione perineale e metastasi ai soli linfonodi regionali. Dopo la chirurgia l’uso della chemioterapia standard è controverso ma alcuni nuovi farmaci (i cosiddetti anti-tirosinchinasici, attivi su questo tumore in circa il 60% dei casi, possono avere la loro efficacia. Questi ultimi farmaci possono essere anche essere utilizzati nel tentativo di diminuire preoperatoriamente le dimensioni dei linfonodi o qualora si siano rilevate metastasi in più sedi, a scopo palliativo. La presenza contestuale di tumore primario e linfonodi regionali colpiti è un fattore che influisce negativamente sulla sopravvivenza (da 12 a 24 mesi). Nei casi in cui è indicata solo l’asportazione del tumore primario (metastasi non rilevate), la sopravvivenza è spesso di oltre 2 anni. “DVM, Prof. Ordinario Clinica Chirurgica Veterinaria, Diplomato ECVS, EBVS® - European Specialist in Small Animal Surgery - (Oncologia Clinica, Chirurgia Oncologica, Chirurgia dei Tessuti Molli)”Prof. Paolo BuraccoAutore #sppb-addon-1719818877863 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877863 img{}#sppb-addon-1719818877864 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877864 img{}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}

Cosa si intende per ostruzione uretrale del gatto? L’ostruzione uretrale del gatto è una patologia ostruttiva acuta a carico dell’uretra, ultimo tratto delle basse vie urinarie, relativamente comune con un tasso di incidenza del 8%. L’ostruzione uretrale del gatto appartiene ad un gruppo di malattie delle basse vie urinarie del gatto denominato FLUTD (dall’inglese Feline Lower Urinary Tract Disease), in cui rientrano la cistite idiopatica felina (FIC) e le infezioni delle vie urinarie (UTI). Se non gestita in modo tempestivo, l’ostruzione uretrale è una condizione potenzialmente fatale. Quali sono le cause dell’ostruzione uretrale del gatto? Le cause di ostruzione uretrale nel gatto sono di due tipologie: Meccaniche (70% dei casi): includono la formazione di calcoli (10% dei casi) o plug (60% dei casi) e, meno frequentemente, di stenosi (restringimenti) all’interno dell’uretra. Funzionali (30% dei casi): rappresentate da spasmo della muscolatura liscia uretrale e/o edema della mucosa (rivestimento interno) uretrale Nel complesso, i plug uretrali sono la causa più comune di ostruzione uretrale del gatto. Si tratta di conglomerati di materiale proteico e cristalli attorno ad una matrice organica costituita da cellule di desquamazione o cellule ematiche. Si ipotizza che processi infiammatori a carico delle basse vie urinarie, come quelli in corso di cistite idiopatica felina, possano giocare un ruolo chiave nella formazione dei plug uretrali favorendo la precipitazione di proteine e lo sfaldamento delle cellule della mucosa uretrale. Inoltre, lo stato infiammatorio a carico di vescica ed uretra può a sua volta indurre l’edema (rigonfiamento) della mucosa uretrale e lo spasmo (contrazione) della muscolatura uretrale portando a un’ostruzione di tipo funzionale. Quali fattori aumentano il rischio di sviluppare l’ostruzione uretrale nel gatto? Sono stati individuati alcuni fattori predisponenti lo sviluppo di ostruzione uretrale nel gatto. Sesso maschile: la malattia è quasi esclusiva di gatti di sesso maschile a causa del diametro inferiore e del decorso maggiormente tortuoso dell’uretra nel gatto rispetto alla gatta Stress ambientali: lo stress di diversa origine è in grado di indurre delle alterazioni di tipo neuro-endocrino in grado di attivare uno stato infiammatorio a carico delle basse vie urinarie Mancato accesso all’esterno: si ipotizza che i gatti esclusivamente indoor siano meno attivi e di conseguenza presentino un numero di urinazioni ridotto favorendo la ritenzione urinaria e la formazione di cristalli e plug nell’urina Obesità Fattori alimentari come il consumo di una dieta esclusivamente secca Quali sono le conseguenze dell’ostruzione uretrale? Il mancato deflusso di urina determina un aumento della pressione idrostatica nelle vie urinarie con direzione retrograda/ascendente. Una volta raggiunta la massima capacità di tensione dei tessuti, questi andranno incontro ad un danno ischemico acuto con conseguente necrosi e morte cellulare. L’aumento della pressione idrostatica si trasmetterà in senso ascendente dalla vescica ai reni causando un danno ischemico acuto con insufficienza renale acuta. Si avrà quindi un accumulo progressivo nel sangue dei prodotti del metabolismo azotato e di elettroliti (come il potassio) normalmente escreti con le urine. Tale accumulo sarà responsabile della comparsa di sintomi clinici sistemici come depressione del sensorio, anoressia e vomito. In caso di grave rialzo di potassio nel sangue (iperpotassiemia) si assisterà a un rallentamento della attività cardiaca con rischio di arresto cardio-respiratorio. Sarà quindi fondamentale riconoscere e trattare tempestivamente l’ostruzione uretrale onde evitare l’insorgenza di grave insufficienza renale e iperpotassiemia. Come si può sospettare l’ostruzione uretrale nel proprio gatto? Non è semplice per il proprietario riconoscere i segni di ostruzione uretrale nel proprio animale, in particolare se in casa sono presenti più gatti o se il gatto è solito urinare all’esterno dell’abitazione. I segni clinici possono essere divisi in segni a carico delle basse vie urinarie e segni sistemici.I sintomi clinici delle basse vie urinarie includono: stranguria (urinazione dolorosa e intermittente a gocce) disuria (difficoltà, irregolarità e dolore durante l’urinazione) dolore addominale I segni clinici sistemici in genere compaiono nei pazienti ostruiti da più di 24 ore. Sono dovuti all’accumulo di tossine uremiche, all’iperpotassiemia e all’alterato stato acido-base del sangue secondari alla insufficienza renale. I sintomi sistemici includono: anoressia (totale perdita di appetito) tachipnea (aumento della frequenza respiratoria) bradicardia (riduzione della frequenza cardiaca) vomito ipotermia (abbassamento della temperatura corporea) La presenza di ipotermia e bradicardia sono forti indicatori della presenza di iperpotassiemia (una grave complicazione). Diagnosi di ostruzione uretrale nel gatto La diagnosi di ostruzione uretrale nel gatto viene effettuata dal medico veterinario solitamente sulla base dei segni clinici riportati dal proprietario e dalla constatazione di una vescica sovradistesa e dolente alla palpazione dell’addome effettuata durante l’esame fisico del gatto. Una volta diagnosticata l’ostruzione uretrale il veterinario dovrà stabilire la gravità del paziente ed individuare e gestire la causa della ostruzione uretrale. Per questo motivo il medico veterinario può richiedere ed effettuare esami ematologici di laboratorio utili per poter valutare lo stato generale del paziente, la presenza ed il grado di insufficienza renale, l’eventuale iperpotassiemia ed utili per stabilire il trattamento terapeutico. Ulteriori esami che il veterinario può richiedere sono l’esame delle urine e l’esame radiografico ed ecografico dell’addome. Queste indagini possono permettere di valutare l’eventuale presenza di calcoli in vescica o in altri tratti delle vie urinarie e l'eventuale, seppur rara, concomitante presenza di infezione delle vie urinarie. L’ostruzione uretrale dovrà essere risolta tramite cateterismo che permette la disostruzione dell’uretra e la fuoriuscita delle urine accumulate in vescica. Una volta risolta l’ostruzione il paziente potrebbe necessitare di una ospedalizzazione di durata variabile in modo da poter monitorare la produzione urinaria e ristabilire il quadro clinico generale. Anche la gestione del dolore mediante somministrazione di analgesici è importante in questo tipo di pazienti. La presenza di cistite, l’ostruzione pregressa, la cateterizzazione, sono tutte condizioni dolorose che richiedono una gestione medica. Fig.1 - Immagine ecografica della vescica urinaria di un gatto con ostruzione uretrale, eseguita dopo disostruzione per cateterismo. Si noti l’ispessimento della parete della vescica (*) indicativo di una concomitante infiammazione della vescica, e la presenza dei 2 piccoli calcoli che sono stati sospinti dall’uretra all’interno della vescica (**) tramite cateterismo e idropulsione. Qual’è la prognosi nella ostruzione uretrale del gatto? Il rischio di recidiva dopo il primo episodio varia dal 15 al 40%.Nonostante le percentuali elevate il veterinario consiglierà di attuare alcuni comportamenti utili per cercare di ridurre il rischio di sviluppo di recidiva. Per esempio: aumentare la quantità di acqua assunta dal proprio gatto per favorire la diuresi prediligere l’utilizzo di una dieta umida che favorisca la produzione di urine diluite arricchimento ambientale per ridurre lo stress e i suoi effetti nocicettivi L'ostruzione uretrale del gatto è una patologia potenzialmente fatale che necessita di essere trattata tempestivamente.Per questo motivo consigliamo di non trascurare nessun atteggiamento di un gatto che mostri difficoltà di urinazione ma di rivolgersi subito al proprio medico veterinario di fiducia.“Med. Vet., Diplomato ACVIM, Diplomato ECVIM-CA, MRCVS, EBVS® - Specialist in Small Animal Internal Medicine”Dr. Fabio ProcoliAutore #sppb-addon-1719818877863 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877863 img{}#sppb-addon-1719818877864 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877864 img{}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}

Cosa si intende per malattia renale cronica del gatto? La malattia renale cronica del gatto (anche nota come CKD dall’inglese chronic kidney disease) è una patologia degenerativa che colpisce solitamente entrambi i reni causandone una perdita di funzionalità di grado variabile. La malattia renale cronica del gatto ha un andamento progressivo e irreversibile, è pertanto fondamentale che la patologia venga riconosciuta precocemente per poterne rallentarne la progressione ed evitare l’instaurarsi di complicazioni sistemiche che possono influire negativamente sulla prognosi nel lungo termine. Quali sono le funzioni principali del rene? Nel gatto come in tutti i mammiferi il rene svolge diverse funzioni vitali come quella di liberare il sangue da tossine e prodotti del metabolismo (che vengono escreti con le urine), regolare il bilancio idrico corporeo, regolare la quantità di sali minerali, partecipare a regolare la pressione sanguigna ed infine quella di produrre ormoni come, ad esempio, l’eritropoietina che stimola la produzione di globuli rossi da parte del midollo osseo. Fortunatamente i reni hanno una grossa riserva funzionale per cui prima che compaiano i segni di insufficienza renale almeno 2/3 della massa renale devono essere andati perduti. Quali sono le cause di malattia renale cronica del gatto? Nella maggiore parte dei casi di malattia renale cronica felina la causa esatta che ha portato alla irreversibile perdita di funzionalità dei reni rimane sconosciuta e si parla pertanto di una eziologia idiopatica. Tuttavia, diverse cause di danno renale cronico sono state individuate nel gatto. Queste includono: Tossine Farmaci Tumori di diversa origine Malattia renale policistica (tipica dei gatti Persiani e simili) Infezioni batteriche (pielonefrite) Infezioni virali Malattie immuno-mediate del rene (glomerulonefriti) Malattie metaboliche (ad esempio l’amiloidosi tipica dei gatti Siamesi, Abissini, Burmesi e di razze orientali a pelo corto) Calcoli renali e ureterali Ipercalcemia (aumento dei livelli di calcio nel sangue) Sarà molto importante quindi, una volta confermata la malattia renale cronica, valutare la presenza di cause predisponenti perché alcune di queste potrebbero essere risolte permettendo di arrestare o quantomeno rallentare la progressione della malattia. Quanto é comune la malattia renale cronica nel gatto? Si stima che circa il 30-50% dei gatti di età superiore ai 10 anni sia affetto da malattia renale cronica. La patologia può colpire gatti di qualsiasi età ma è solitamente diagnosticata in gatti di età geriatrica (superiore a 7 anni). Seppur gatti di qualsiasi razza e anche gatti comuni europei soffrano di malattia renale cronica, alcune razze feline sono maggiormente a rischio come Maine coon, Abissino, Blu di Russia, Burmese e Siamese. Non è stata invece riscontrata una predisposizione legata al sesso. Quali sono i sintomi clinici associati alla malattia renale cronica del gatto? I sintomi clinici in corso di malattia renale cronica variano con il grado e durata della patologia, con la presenza di patologie concomitanti e dalla comparsa o meno di complicazioni sistemiche.Essendo una patologia progressiva, i sintomi clinici a cui fare attenzione, negli stadi iniziali sono assenti o molto lievi mentre tendono a diventare maggiormente manifesti con l’avanzare della malattia.I sintomi clinici più comuni ma poco specifici (ovvero che possono essere causati da altre patologie) includono: Perdita di peso Perdita di appetito Abbattimento Aumento della sete (polidipsia) Aumento della urinazione (poliuria) I sintomi clinici meno comuni o associati agli stadi più gravi/avanzati della malattia includono: Alitosi Vomito Debolezza Può il medico veterinario sospettare durante l’esame fisico la presenza di malattia renale cronica? L’esame fisico di gatti con affetti da malattia renale cronica di stadio iniziale è spesso completamente nella norma.Le alterazioni riscontrabili negli stadi più avanzati o cronici della malattia includono: Scarse condizioni corporee e muscolari Pelo di scarsa qualità Stomatite ed ulcere linguali Alitosi uremica Disidratazione Pallore delle mucose Aumento della pressione sanguigna Riduzione di dimensione dei reni apprezzabile alla palpazione dell’addome Come viene diagnosticata la malattia renale cronica del gatto? Tradizionalmente la diagnosi di malattia renale cronica viene emessa attraverso un esame del sangue con il ritrovamento di un aumento dei livelli ematici di urea e creatinina (due prodotti del metabolismo proteico che vengono eliminati dai reni) e attraverso un esame delle urine con la dimostrazione di urine non adeguatamente concentrate (con peso specifico minore di 1.030). Vista l’alta prevalenza della malattia renale cronica nella popolazione felina geriatrica diventa fondamentale non sottovalutare la comparsa di sintomi vaghi e aspecifici come la perdita di peso o la leggera perdita di appetito in gatti di età superiore a 7 anni. In presenza di questi sintomi o meglio routinariamente in gatti di età maggiore di 7 anni, è consigliabile far visitare il proprio gatto dal vostro veterinario di fiducia che potrebbe richiedere uno screening precauzionale e l’esecuzione di esami del sangue e delle urine per escludere la presenza di malattia renale cronica o, se confermata, permettere una gestione terapeutica mirata che aiuti a prevenire la progressione della malattia. Una volta sospettata o confermata la presenza di malattia renale cronica il veterinario potrà eseguire ulteriori indagini diagnostiche per identificare l’eventuale presenza di cause sottostanti potenzialmente risolvibili e per stadiare la malattia renale cronica stessa (ovvero determinarne la gravità), individuare la presenza di complicazioni sistemiche o la presenza di fattori prognostici negativi. Tra le indagini diagnostiche ulteriori che il veterinario può richiedere vi sono: Profilo emocromocitometrico: per valutare la presenza di anemia significativa, nota complicazione della malattia renale cronica dovuta a una ridotta produzione da parte del rene dell’ormone eritropoietina Profilo biochimico completo (in aggiunta a urea, creatinina e SDMA): per valutare la presenza di iperfosfatemia (aumento della concentrazione di fosforo), ipercalcemia o ipocalcemia (aumento o diminuzione del calcio ematico), ipopotassiemia (diminuzione del potassio ematico) Esame fisico-chimico e del sedimento delle urine: per valutare la presenza di sangue, cristalli, cilindri o batteri o una perdita di proteine con le urine (proteinuria) Esame colturale delle urine: per valutare la presenza di una infezione delle basse vie urinarie o dei reni (pielonefrite), quest’ultima possibile causa di malattia renale cronica Determinazione della tiroxina sierica: l’ipertiroidismo felino è un’altra patologia tipica del gatto geriatrico che può interferire con i test diagnostici della malattia renale cronica e la cui presenza va esclusa sistematicamente oltre i 7 anni di età Diagnostica per immagini: fra le varie procedure di diagnostica per immagini l’ecografia addominale è la metodica di scelta in quanto permette di valutare le dimensioni e architettura dei reni e confermare la presenza di una nefropatia cronica di diversa natura e di valutare il resto dell’apparato urinario e di rilevare la presenza di calcoli renali o ureterali che possono contribuire al danno renale. Quali sono le alterazioni ecografiche tipiche della malattia renale cronica del gatto? In corso di malattia renale cronica i reni possono e perdere la normale distinzione tra la parte più esterna (la corticale) e quella più interna (la midollare) (Fig 1-2), possono presentare la formazione di mineralizzazioni al loro interno, possono apparire ridotti di dimensioni e in alcuni casi estremi possono perdere del tutto la loro architettura come nel caso di tumori o di malattia policistica.Inoltre, l’esame ecografico addominale in un gatto con malattia renale cronica può rivelare segni contestuali di infezione (pielonefriti, Fig. 3) o di urolitiasi (calcoli renali, ureterali). Fig. 1 - Immagine ecografica di un rene normale in cui è possibile la parte esterna (corticale, C) dalla parte interna (midollare, M)Fig. 2 - Ecografia di un gatto con malattia renale cronica avanzata. Si noti la perdita della normale distinzione cortico-midollare (*), l’aspetto irregolare del profilo renale (**) e la lieve quantità di versamento perirenale (freccia).Fig. 3 - Immagine ecografica di un gatto con malattia renale cronica dove si apprezza, tra i rilievi principali, una lieve dilatazione del bacinetto renale compatibile con una infezione batterica renale (pielonefrite). Quali sono le complicazioni note della malattia renale cronica? Tra le complicazioni secondarie alla malattia renale cronica, le più note includono: Anemia cronica secondaria alla ridotta produzione renale dell’ormone eritropoietina. L’anemia se molto grave può peggiorare la qualità di vita del gatto o compromettere la sua sopravvivenza. Alterazione dell’equilibrio acido-base del sangue: l’alterazione dei meccanismi di escrezione e riassorbimento renale in corso di malattia renale cronica può portare a squilibri minerali con conseguente acidificazione del sangue (acidosi metabolica) che se grave può comportare segni clinici importanti. Ipertensione sistemica: la malattia renale cronica può predisporre attraverso diversi meccanismi all’aumento della pressione sanguigna che se grave e non trattata può provocare danno ischemico ai reni stessi ma anche a livello cerebrale, cardiaco e oculare. Qual è la prognosi in corso di malattia renale cronica del gatto? La prognosi di un gatto con malattia renale cronica dipenderà dallo stadio della malattia, dal suo riconoscimento precoce e dal susseguente inizio di una gestione terapeutica adeguata (solitamente multimodale) e dalla eventuale presenza di complicazioni o patologie concomitanti. Nel complesso, se diagnosticata precocemente e trattata adeguatamente la patologia consente al gatto di vivere buona qualità di vita anche nel lungo termine, con un tasso di mortalità < 15%. “Med. Vet., Diplomato ACVIM, Diplomato ECVIM-CA, MRCVS, EBVS® - Specialist in Small Animal Internal Medicine”Dr. Fabio ProcoliAutore #sppb-addon-1719818877863 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877863 img{}#sppb-addon-1719818877864 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877864 img{}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}
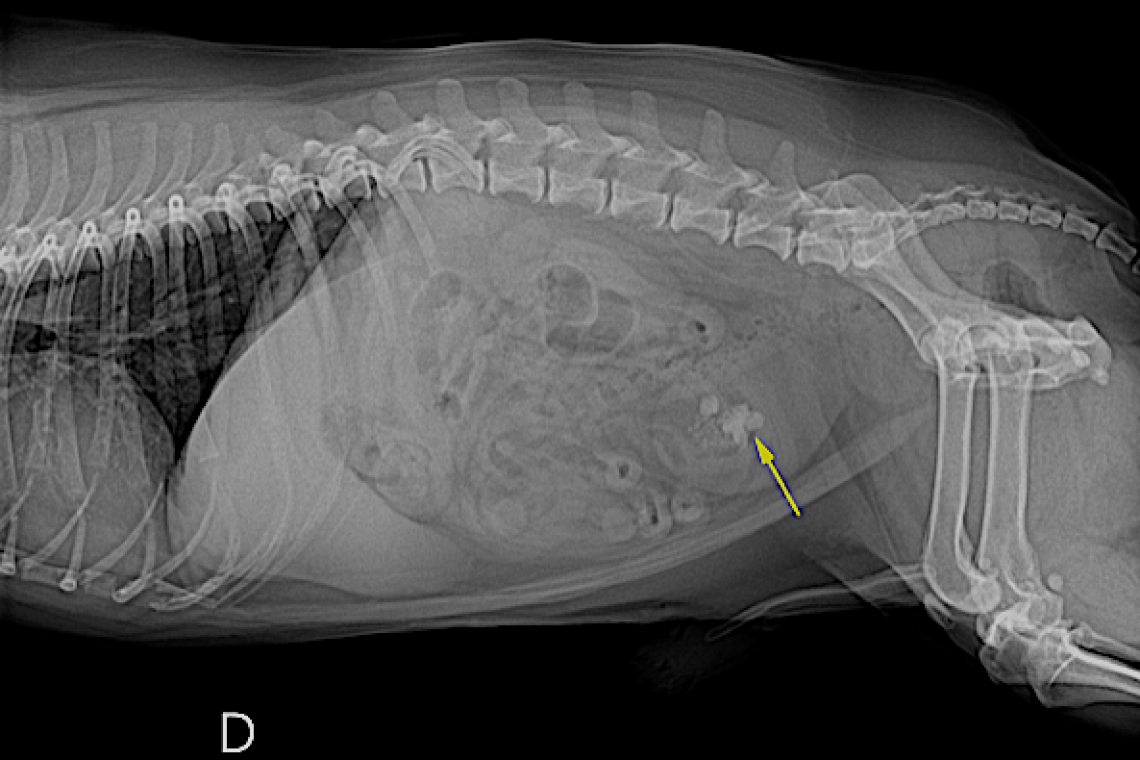
Cosa si intende per urolitiasi? Il termine urolitiasi si riferisce alla presenza di calcoli nell’apparato urinario che va dal bacinetto renale (nefrolitiasi) fino all’uretra (uretrolitiasi) passando per ureteri (ureterolitiasi) e vescica urinaria (urocistolitiasi). Cosa causa l’urolitiasi? Tendenzialmente l’urolitiasi insorge quando le urine diventano eccessivamente sature di minerali che in determinate condizioni chimico-fisiche precipitano, cristallizzano e si aggregano fino a portare alla formazione del calcolo urinario. L’eccessiva saturazione delle urine avviene fondamentalmente per una eccessiva produzione e/o escrezione di determinati minerali nelle urine o per la carenza di sostanze naturalmente inibenti la precipitazione e formazione di cristalli. Diverse sono le cause predisponenti la formazione di calcoli urinari. Tra queste si annoverano difetti genetici, fattori alimentari, malattie metaboliche, malattie endocrine, presenza di detriti cellulari e infezioni del tratto urinario. Come è composto un calcolo urinario? Strutturalmente il calcolo urinario è costituito da un nucleo centrale, costituito da matrice organica, e da un guscio esterno composto da uno o più sali minerali. La percentuale relativa di sali minerali del guscio determina il tipo del calcolo che potrà essere puro, se costituito da 1 solo minerale, o misto se costituito da 2 o più minerali. La composizione del calcolo urinario inoltre determinerà alcune sue caratteristiche intrinseche come la forma e radio-opacità o radio-lucentezza e il numero. Determinare la composizione dei calcoli è fondamentale in quanto permette di identificare la presenza di cause predisponenti e di definire la strategia terapeutica più adatta. Quali sono i tipi di calcolo urinario più comune nel cane e nel gatto? I tipi di calcoli urinari più comuni nel cane e nel gatto sono i seguenti (dai più comuni ai meno frequenti): CALCOLI DI STRUVITE questi calcoli urinari sono composti da cristalli di fosfato idrato di ammonio e magnesio. Si formano in presenza di urine soprasature di ammonio, fosfato e magnesio. Questo può avvenire in corso di infezioni batteriche delle vie urinarie (struvite infezione indotta) o in presenza di urine sterili (struvite sterile). I calcoli urinari di struvite infezione indotta sono più comuni nel cane mentre quelli di struvite sterile sono più comuni nel gatto. I calcoli di struvite possono essere disciolti attraverso una gestione dietetica e medica senza ricorrere a rimozione chirurgica o mininvasiva. Struvite infezione indotta. Si ritrova con maggiore incidenza nei cani di qualsiasi età e nei gatti di età inferiore ad 1 anno o maggiore di 10 anni. Non sembrano esserci nel gatto predisposizioni di razza o sesso al contrario del cane dove sono più colpite le femmine, probabilmente a causa di una maggiore predisposizione allo sviluppo di infezioni urinarie. Infatti, questo tipo di uroliti sono associati a infezioni delle vie urinarie ad opera di batteri ureasi produttori come Staphylococcus spp, Enterococcus spp, e Proteus spp. Struvite sterile. Colpisce soprattutto gatti di età compresa tra gli 1 e i 10 anni, senza predisposizione di sesso. Sono stati individuati alcuni fattori predisponenti alla formazione di questi calcoli, tra cui la somministrazione di diete ad alto contenuto in magnesio, predisposizione genetica individuale da soggetto a soggetto e urine con pH alcalino (pH>7). Anche il ridotto consumo di acqua e un minor volume di urine prodotte sembrano predisporre la formazione dei calcoli. CALCILI DI OSSALATO DI CALCIO Questi calcoli urinari rappresentano circa il 40-50% di tutti gli uroliti del cane e del gatto. Alcune razze di cani e gatti sembrano essere predisposte. Nel cane, razze di piccola taglia come lo Schnauzer nano, lo Shih-tzu e lo Yorkshire terrier sono particolarmente predisposte. Nel gatto, il Persiano, l’Himalaiano e il Burmese sono sovrarappresentati. Due fattori di rischio per la formazione di calcoli di ossalato di calcio sono l’elevata concentrazione di ossalato e calcio nelle urine e la produzione di urine acide (con pH urinario < 6.6). Gli uroliti di ossalato di calcio non possono essere dissolti mediante terapia medica, pertanto l’approccio chirurgico o la retropulsione in vescica rappresentano l’unico approccio possibile. Inoltre, questo tipo di uroliti ha la tendenza a recidivare. CALCOLI DI AMMONIO DI URATO Questi calcoli urinari rappresentano la terza tipologia di uroliti più frequentemente riscontrata nel cane e nel gatto. Questi calcoli formano in presenza di urine soprasature di cristalli di urato e ammonio, che a loro volta si formano in presenza di elevate concentrazioni di acido urico nelle urine. Alcune razze di cane come il Dalmata e il Bulldog Inglese sono geneticamente predisposte alla eccessiva produzione ed escrezione di acido urico nelle urine e quindi alla formazione di cristalli e calcoli di urato d’ammonio.Un altro fattore predisponente la formazione di questi calcoli è la presenza di patologie del fegato con insufficienza d’organo (come accade nel caso di anomalie vascolari epatiche congenite). La dissoluzione medica di questi uroliti in concomitanza a patologie epatiche non è possibile la risoluzione chirurgica rimane l’unica scelta nei pazienti sintomatici. Nei casi di urolitiasi in assenza di patologia epatica la dissoluzione medica può essere tentata. CALCOLI DI CISTINA Questi calcoli urinari si riscontrano in cani e gatti affetti da cistinuria, un disordine metabolico congenito caratterizzato da un’eccessiva escrezione di cistina (insieme ad altri aminoacidi come lisina, ornitina e arginina) nelle urine. Non sono riportate predisposizioni di razza o sesso, ma i gatti Siamesi sembrano essere più colpiti. Come per i calcoli di struvite, anche in questo caso la dissoluzione mediante terapia dietetica e medica è possibile così come è possibile prevenirne la futura formazione. Quali sono i sintomi clinici che possono far sospettare l’urolitiasi nel cane e nel gatto? Il corredo sintomatico in corso di urolitiasi dipenderà dalla localizzazione del calcolo nell’apparato urinario, da numero e dimensioni, dalla insorgenza di ostruzione delle vie urinarie alte (es. ureteri) o basse (uretra) e dalla presenza o meno di fattori predisponenti come, ad esempio, l’infezione delle vie urinarie. Il sospetto di urolitiasi può insorgere in seguito alla comparsa di segni clinici a carico delle vie urinarie quali: Ematuria (presenza di sangue nelle urine) Pollachiuria (aumento del numero delle urinazioni) Stranguria (urinazione dolorosa) Disuria (urinazione difficoltosa) È importante ricordare che tali sintomi, sebbene riscontrabili in corso di urolitiasi, non sono specifici per tale patologia e che l’urolitiasi può insorgere in assenza di sintomi clinici. Pertanto, è necessario conoscerne l’esistenza, la predisposizione di razza (soprattutto nel cane) e eseguire un iter diagnostico specifico al fine di confermarne la presenza, stabilirne la natura, la localizzazione e l’estensione e di valutare la presenza di avvenuta o prossima ostruzione delle vie urinarie e di cause sottostanti/predisponenti. Come posso confermare la diagnosi di urolitiasi nel cane e nel gatto? La conferma della presenza di calcoli urinari solitamente avviene mediante tecniche di diagnostica per immagini che permettono, inoltre, di definirne localizzazione, dimensione, forma, densità e numero. In aggiunta l’esame delle urine aiuta a definire la natura del calcolo urinario e a identificare la presenza di fattori predisponenti.Gli esami ematici di laboratorio sono altresì importanti nel valutare la presenza di una patologia sottostante che può aver favorito l’insorgenza dell’urolitiasi e che andrà trattata per ottimizzare la gestione terapeutica del calcolo urinario. Inoltre, gli esami ematici permettono di valutare l’insorgenza di insufficienza renale secondaria a ostruzione delle vie urinarie o infezione renale secondaria alla presenza di un calcolo. La radiografia addominale è in genere il primo strumento diagnostico utile per individuare la presenza di calcoli radiopachi (con composizione tale da renderli visibili radiograficamente) come quelli di struvite e ossalato di calcio (Fig. 1). Nel caso di uroliti radiolucenti (non visibili radiograficamente) o di piccole dimensioni (minoridi 3 mm) saranno necessarie altre metodiche diagnostiche come la radiografia con mezzo di contrasto, sia positivo che negativo, o l’ecografia. Fig. 1 ed immagine di copertina - Radiografia addominale di un cane che evidenzia la presenza di numerosi calcoli (freccia) radio-opachi rotondeggianti e di dimensioni variabili all’interno della vescica urinaria. L’esame del sedimento urinario ha in seguito confermato la presenza di numerosi cristalli di struvite.L’esame ecografico permette di valutare non solo la presenza e localizzazione dei calcoli ma anche di determinare la presenza di avvenuta o prossima ostruzione di un tratto dell’apparato urinario (Fig. 2).Fig. 2 - Immagine ecografica addominale in un cane maschio intero che evidenzia la presenza di un calcolo urinario (freccia) all’interno della uretra prostatica.L’esame del sedimento urinario è particolarmente utile nei pazienti in cui si sospetta o è stata riscontrata la presenza di un calcolo urinario.L’esame del sedimento urinario può rilevare la presenza di cristalli di diverso tipo (Fig. da 3 a 7) che può indicare la presenza di calcoli urinari e può aiutare a stabilire la natura del calcolo stesso, fondamentale per l’impostazione di una terapia mirata. Tuttavia, va precisato che il riscontro di cristalli all’esame del sedimento urinario non equivale a una diagnosi certa di urolitiasi così come l’assenza di cristalli urinari all’esame del sedimento urinario non esclude la presenza di calcoli urinari. Foto 3 - Cristalli di StruviteFoto 4 - Cristalli di Ossalato di Calcio diidratoFoto 5 - Cristalli di Ossalato di Calcio monoidrato (forma più rara)Foto 6 - Cristalli di Urato di AmmonioFoto 7 - Cristalli di CistinaL’esame fisico-chimico delle urine permette di determinare il peso specifico urinario e il pH fornendo importanti informazioni sulla probabile composizione chimica del calcolo urinario. Ad esempio, il ritrovamento di un pH delle urine < 7.0 potrebbe indicare che i calcoli ritrovati radiograficamente saranno di ossalato di calcio o cistina, in quanto questi richiedono un ambiente acido per precipitare e aggregarsi. Al contrario, il ritrovamento di un pH delle urine > 7.0 (alcalino) potrebbe indicare che i calcoli sono di struvite. Infine, l’esame colturale delle urine è utile per identificare la presenza di batteri ureasi-produttori in grado di alcalinizzare le urine e facilitare la formazione di uroliti di struvite (infezione indotta). In aggiunta, infezioni batteriche possono insorgere secondariamente alla presenza di calcoli urinari contribuendo ai sintomi clinici e complicando la gestione dell’urolitiasi.“Med. Vet., Diplomato ACVIM, Diplomato ECVIM-CA, MRCVS, EBVS® - Specialist in Small Animal Internal Medicine”Dr. Fabio ProcoliAutore #sppb-addon-1719818877863 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877863 img{}#sppb-addon-1719818877864 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877864 img{}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}

Che cosa si intende per pancreatite del gatto? La pancreatite del gatto è un processo infiammatorio a carico del pancreas esocrino. Il pancreas è un organo addominale situato in prossimità dell’intestino del tenue che, da un punto funzionale, viene distinto in due parti: una endocrina ed una esocrina. La parte endocrina è costituita da cellule specializzate organizzate in isolotti (cosiddetti del Langherans) che producono una serie di ormoni immessi in circolo per influenzare l’attività di diversi organi. Tra questi ormoni spicca l’insulina, l’ormone deputato al controllo dei livelli ematici di glucosio. La parte esocrina del pancreas (quella colpita dalla pancreatite) è invece costituita da cellule epiteliali organizzate in acini la cui funzione principale è quella di sintetizzare e rilasciare nell’intestino tenue diverse sostanze, dette enzimi, in grado di permettere la digestione dei principali macronutrienti della dieta ovvero carboidrati, lipidi e proteine. In corso di pancreatite del gatto il pancreas esocrino viene infiltrato da cellule del sistema immunitario di diverso tipo (neutrofili, linfociti e plasmacellule). Questo comporta un danno alle cellule epiteliali con la perdita di enzimi digestivi all’interno del pancreas stesso con conseguente danno tissutale che può estendersi agli organi adiacenti al pancreas (intestino, fegato e vie biliari) e al grasso addominale circostante. Quanti tipi di pancreatite esistono nel gatto? La pancreatite del gatto viene distinta in acuta e cronica. Quest’ultima di gran lunga più frequente. La distinzione tra la forma acuta e cronica della malattia da un punto di vista clinico, di laboratorio e diagnostico non è sempre facile in quanto le due forme possono essere perfettamente sovrapponibili. In questi casi, la distinzione può essere fatta solo attraverso l’ausilio dell’esame istologico su biopsie pancreatiche e la dimostrazione o meno di rilievi tipici della infiammazione cronica. Detto questo, le forme acute gravi sono facilmente riconoscibili per la rapida insorgenza e la gravità del quadro clinico rispetto all’insorgenza più lenta e subdola della pancreatite cronica. Cosa causa la pancreatite del gatto? La causa esatta della pancreatite è sconosciuta. Nel gatto non sono state riportate predisposizioni di razza, sesso o età. Nel 95% dei casi non viene identificato un fattore scatenante per cui la patologia viene definita idiopatica. Nel caso della pancreatite cronica si sospetta una disfunzione del sistema immunitario con un ruolo giocato dalla flora batterica intestinale in grado di colonizzare il pancreas e stimolare una risposta aberrante del sistema immunitario. Nel caso della pancreatite acuta si assiste a un’attivazione precoce degli enzimi pancreatici ancora all’interno del tessuto pancreatico, con conseguente danno tissutale e richiamo di cellule infiammatorie. Alcuni fattori sono stati proposti come potenzialmente predisponenti di pancreatite acuta: Diete ricche di grassi. Si è vista in alcuni casi che vi è maggiore incidenza di pancreatite nei gatti in sovrappeso o sottoposti a diete con alto contenuto di grassi. Infezioni sostenute da protozoi (Toxoplasma gondii) o virus (parvovirus felino, coronavirus, herpesvirus e calicivirus). Anestesia generale prolungata con calo pressorio e riduzione della perfusione sanguigna e danno ischemico al pancreas. Traumi Manipolazione chirurgica del pancreas o del duodeno (annesso al pancreas) Quali sono i segni clinici di pancreatite nel gatto? I segni clinici riportati in corso di pancreatite nel gatto sono piuttosto aspecifici e possono essere presenti in entrambe le forme acuta e cronica della patologia. Il corredo sintomatico dipenderà dalla durata e gravità della malattia, dalla presenza di patologie concomitanti (ad esempio a carico del fegato, delle vie biliari e dell’intestino) e dalla presenza di complicazioni (ad esempio la sindrome della lipidosi epatica). I sintomi più comunemente riportati dal proprietario includono: Anoressia più o meno prolungata (forma acuta e cronica) Letargia (forma acuta) Sintomi gastrointestinali come nausea, ipersalivazione, vomito, diarrea (forma acuta e cronica) Perdita di peso (forma cronica) Quali sono i rilievi riscontrati all’esame fisico nei gatti con pancreatite? I rilievi dell’esame fisico in gatti con pancreatite dipenderanno anche in questo caso dalla durata e gravità della malattia, dalla presenza di patologie concomitanti e/o di complicazioni. I rilievi possibili includono: Depressione/letargia (forma acuta > cronica) Condizioni corporee scadenti (forma cronica) Disidratazione (forma acuta e cronica) Febbre (forma acuta) Ittero (colorazione giallastra delle sclere e delle mucose, forma acuta) Dolore addominale (forma acuta) Come si effettua diagnosi di pancreatite nel gatto? Per la diagnosi definitiva di pancreatite del gatto e la distinzione tra forma acuta e cronica può essere effettuata solo tramite esame istologico su biopsie di pancreas raccolte per via laparoscopica o chirurgica. La presenza di necrosi tissutale (forma acuta) o fibrosi con perdita di tessuto (forma cronica) e il grado e tipologia di infiltrato infiammatorio (neutrofili nella forma acuta ma linfocitici e plasmacellule nella forma cronica) permettono la diagnosi definitiva. Tuttavia, viste la relativa invasività della procedura, le condizioni cliniche spesso poco stabili dei gatti affetti (forma acuta) e per la presenza di forme subcliniche o paucisintomatiche l’esame istologico viene raramente eseguito. In questo caso la diagnosi rimarrà presunta con un grado di affidabilità variabile ed il Medico Veterinario potrà basarsi sull’integrazione di sintomi clinici, esame fisico, esami di laboratorio (di base e specifici) ed ecografia addominale. Esami di laboratorio di base. Le alterazioni in corso di pancreatite del gatto sono aspecifiche e in comune a diverse patologie per cui non permettono di emettere una diagnosi presunta. Il ruolo di questi esami è principalmente quello di valutare la gravità del quadro clinico, la presenza di patologie concomitanti e/o la presenza di eventuali fattori prognostici negativi. Possibili rilievi, soprattutto nella forma acuta di pancreatite, includono anemia, riduzione o aumento dei globuli bianchi, riduzione del glucosio, riduzione di elettroliti come sodio, potassio e calcio, aumento dei valori epatici e di bilirubina quest’ultima indicativa di una possibile ostruzione delle vie biliari. Test specifici di infiammazione pancreatica. Questi test includono la lipasi pancreatica specifica e la DGGR lipasi che fungono da marker indiretto di infiammazione pancreatica. Infatti, quando il pancreas è infiammato o danneggiato, le vescicole contenenti gli enzimi pancreatici (inclusa la lipasi) si rompono e il loro contenuto viene riassorbito dal circolo ematico permettendo la loro misurazione. Ecografia addominale. Questa è la modalità di diagnostica per immagini di scelta per la diagnosi presunta di pancreatite ed è superiore alla radiografia (Figura 1).L’esame ecografico permette di valutare non solo il pancreas ma anche quegli organi spesso coinvolti da processi patologici in corso di pancreatite come fegato, vie biliari e intestino.Inoltre, se eseguita da operatori esperti è possibile distinguere la forma acuta da quella cronica.Infine, l’ecografia permette di raccogliere dei campioni cellulari di pancreas (per ago infissione) da sottoporre all’esame citologico con la possibilità permettere di raggiungere una diagnosi più affidabile di pancreatite del gatto. Figura 1 - Radiografia addominale di un gatto con pancreatite acuta grave. Si apprezza la perdita di dettaglio nell’addome craniale nella regione del pancreas (freccia) causata dalla reattività del grasso e dei tessuti circostanti il pancreas. Nella pancreatite cronica il pancreas risulta ridotto di dimensioni, fibrotico e può mostrare una dilatazione del dotto pancreatico.Nella pancreatite acuta il pancreas appare aumentato di volume, rigonfio e i tessuti e il grasso circostanti risultano reattivi. Inoltre, è possibile riscontrare la presenza di liquido libero addominale dovuto all’infiammazione (Figura 2). Figura 2 - Immagine ecografica di pancreatite acuta nel gatto. È presente reattività del grasso circostante il pancreas (freccia gialla). Quest’ultimo appare aumentato di volume e edematoso (freccia rossa).Qual è la prognosi di pancreatite nel gatto? La prognosi in corso di pancreatite del gatto dipenderà da diversi fattori come forma, gravità, presenza di patologie concomitanti e/o di complicazioni. Quest’ultime sono più comuni in corso di pancreatite acuta grave e includono disturbi della coagulazione con sanguinamenti spontanei, sepsi, insufficienza del fegato associata a infarcimento di grasso (lipidosi epatica) danno acuto multiorgano (reni, fegato, polmoni), ostruzione delle vie biliari e comparsa di diabete mellito. Nei casi più gravi la prognosi è riservata e il rischio di mortalità è elevato (fino al 40%). I gatti con pancreatite acuta di grado lieve-moderata o cronica hanno invece una prognosi migliore con rischio di mortalità basso. Complicazioni della pancreatite cronica includono malnutrizione e progressiva perdita di funzione esocrina del pancreas (insufficienza del pancreas esocrino, EPI), quest’ultima sottovalutata e di conseguenza sotto-diagnosticata.“Med. Vet., Diplomato ACVIM, Diplomato ECVIM-CA, MRCVS, EBVS® - Specialist in Small Animal Internal Medicine”Dr. Fabio ProcoliAutore #sppb-addon-1719818877863 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877863 img{}#sppb-addon-1719818877864 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877864 img{}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}

Che cos’è il collasso tracheale del cane? Il collasso tracheale è una patologia cronica, progressiva e irreversibile che colpisce la trachea del cane. La trachea è la porzione dell’apparato respiratorio che mette in comunicazione le vie aeree superiori (cavità nasali, rino-faringe e laringe) con quelle inferiori all’interno dei polmoni (bronchi principali e secondari, bronchioli e alveoli). La trachea ha una forma tubulare ed è costituita da una serie di strutture cartilaginee elastiche a forma di C (con la parte aperta della C diretta verso l’alto), chiamate anelli tracheali, ricoperte dorsalmente da una membrana elastica (che completa la C dell’anello tracheale). Questa struttura le conferisce rigidità, resistenza e una certa flessibilità che permettono il passaggio di aria ai e dai polmoni durante le fasi della respirazione e l’attività fisica. Internamente, la trachea è rivestita da uno strato di cellule munite di ciglia che permettono l’espulsione di impurità dalle vie respiratorie inferiori. Se gli anelli tracheali perdono la loro normale conformazione e rigidità tendono a indebolirsi e diventare più piatti (collasso tracheale) causando una vera e propria ostruzione dinamica al flusso d’aria. Questa deformazione può manifestarsi in forme più o meno gravi ed essere associata o meno alla concomitante alterazione dei bronchi principali (Foto 1). Foto 1. - Classificazione dei diversi gradi di collasso tracheale nel cane in base alla percentuale di riduzione del calibro interno. Cosa causa il collasso tracheale nel cane? Nella maggior parte dei casi il collasso tracheale è dovuto ad una degenerazione cronica e progressiva nel tempo degli anelli tracheali che perdono la loro elasticità appiattendosi su loro stessi e ostruendo il lume (cavità interna) della trachea. Questa forma di collasso tracheale colpisce cani in età media-avanzata. Più raramente, il collasso tracheale è causato da una malformazione congenita degli anelli tracheali che appaiono deformati e meno elastici con conseguente riduzione del calibro interno della trachea. Questa forma di collasso tracheale si manifesta in età giovanile. Quali sono fattori predispongono al collasso tracheale nel cane? La causa esatta della patologia è sconosciuta. Tuttavia, diversi sono i fattori riportati come predisponenti o contribuenti al collasso tracheale e diversi sono i disturbi presenti in associazione al collasso tracheale nel cane. I più importanti di questi sono: Predisposizione genetica (di razza): il collasso tracheale è quasi esclusivamente riportato in razze di piccola taglia o toy. Particolarmente predisposti sono lo Yorkshire terrier, il Volpino di Pomerania, il Chihuahua, il Barboncino e il Maltese. Obesità Patologie cardiache Malattie del cavo orale Inalazione di sostanze irritanti Infezioni delle vie respiratorie Quali sono i sintomi tipici del collasso tracheale nel cane? I sintomi del collasso tracheale variano a seconda della gravità della patologia e della presenza di complicazioni o patologie concomitanti (come cardiopatie o broncopatie croniche). Il segno clinico più frequente nei cani con collasso tracheale è la tosse. Quest’ultima è secca, profonda (“a verso d’anatra”) e spesso parossistica (in accessi violenti). La tosse solitamente peggiora con l’eccitamento, lo stress, l’esercizio fisico o con il caldo. Nelle forme più gravi di collasso tracheale i cani affetti possono presentare intolleranza all’esercizio fisico, abbattimento e improvvisa difficoltà respiratoria. Quali sono le complicazioni del collasso tracheale? Nei casi più gravi o trascurati, il collasso tracheale può indurre una insufficienza respiratoria con cianosi, ipertensione polmonare con sincope (svenimento) e insufficienza del cuore destro. Se non riconosciute e prontamente trattate queste complicazioni possono diventare fatali. Come viene emessa la diagnosi di collasso tracheale nel cane? Il sospetto di collasso tracheale viene emesso in cani di razza ed età a rischio in presenza di sintomi clinici compatibili. La diagnosi definitiva prevede la dimostrazione dell’appiattimento degli anelli tracheali, la determinazione della gravità (percentuale di collasso), la sua localizzazione a un tratto o a tutta la tracheale (collasso segmentale vs diffuso) e la dipendenza o meno dalle fasi respiratorie (collasso dinamico vs collasso statico). Le indagini diagnostiche che il Medico Veterinario potrà richiedere sono la radiografia, l’endoscopia e la fluoroscopia (Foto 2). Foto 2. - Radiografia toracica laterale in un cane Pinscher di 5 anni con collasso tracheale cervicale di IV grado e intratoracico di II grado (freccia rossa). Si noti il grave restringimento del calibro tracheale che in condizioni normali dovrebbe apparire come un tubo omogeneo radiotrasparente (ovvero nero per la presenza di aria). Di queste procedure diagnostiche, l’endoscopia delle vie aeree rappresenta l’esame più completo in quanto permette di valutare l’estensione del collasso tracheale (se diffusamente interessata o solo una porzione), la gravità (intesa come percentuale di restringimento del lume tracheale) e il tipo di collasso (Foto 3).L’endoscopia permette altresì di identificare patologie delle basse vie respiratorie spesso concomitanti, quali broncopatie croniche, collasso bronchiale e broncomalacia. Foto 3 e in copertina - Vista endoscopica della trachea cervicale in un cane Chihuahua di 12 anni con grave collasso tracheale (IV grado) del tratto cervicale. Le pareti del lume tracheale collassano a tal punto da toccarsi, creando una grave ostruzione al flusso d’aria (immagini endoscopiche per gentile concessione del Dott. Davide De Lorenzi esperto MYLAV). Quali sono le terapie per il collasso tracheale? La terapia del collasso tracheale che il Veterinario potrà prescrivere dipenderà dal grado e tipo di collasso e dalla presenza o meno di patologie concomitanti e complicazioni. Spesso, si tratta di una terapia multimodale che include sia la riduzione o meglio eliminazione dei fattori predisponenti, che una terapia farmacologica (antinfiammatori, farmaci antitussivi e tranquillanti). Nei casi più gravi il Medico Veterinario potrà consigliare l’applicazione di uno stent (divaricatore) all’interno della trachea (Foto 4). Foto 4 - Radiografia laterale dello stesso cane della foto 2 dopo l’applicazione di uno stent endotracheale (frecce rosse) nel tratto cervicale e toracico. Da notare come, grazie allo stent, venga ottenuto il ritorno a un calibro normale del lume endotracheale. Il collasso tracheale è una malattia progressiva per cui la terapia ha lo scopo di controllare i sintomi clinici ed evitare o ritardare eventuali complicazioni per consentire una qualità di vita adeguata. “Med. Vet., Diplomato ACVIM, Diplomato ECVIM-CA, MRCVS, EBVS® - Specialist in Small Animal Internal Medicine”Dr. Fabio ProcoliAutore #sppb-addon-1719818877863 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877863 img{}#sppb-addon-1719818877864 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877864 img{}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}

