La parvovirosi è una malattia infettiva altamente contagiosa, ad eziologia virale, che provoca una grave gastroenterite. Tale patologia, nei i cuccioli al di sotto dei 6 mesi di età, è spesso fatale. L’agente infettivo è il parvovirus canino (CPV) di tipo 2, da non confondere con il parvovirus canino di tipo 1 che è generalmente meno pericoloso e può dare forme gastroenteriche più lievi, miocarditi e polmoniti nei cuccioli di 1-3 settimane di età. L’infezione da parvovirus rappresenta probabilmente la più comune e grave causa di enterite del cane. Da quando nel 1978, il parvovirus canino venne identificato per la prima volta come agente eziologioco di enterite nel cane, tale patologia, a diffusione mondiale, ha assunto una notevole importanza in ambito veterinario. Il parvovirus canino ha delle caratteristiche che lo rendono particolarmente pericoloso: ha un ciclo oro-fecale, è quindi necessario che un cane infetto elimini il virus con le feci, che si disperda nell’ambiente e che un altro soggetto ne venga a contatto (Figura 1) è molto resistente nell’ambiente, bisogna quindi fare molta attenzione ad ambienti e materiali contaminanti (vestiti, oggetti, pelo del cane, pavimento) ha uno spiccato tropismo per le cellule in rapida replicazione, in particolar modo le cellule dell’intestino, quelle del midollo osseo e quelle del sistema linfatico è altamente contagioso Queste caratteristiche fanno sì che si possano facilmente innescare dei cicli endemici con alto tasso di mortalità all’interno di canili, pensioni per cani o negozi di animali. L’infezione può anche avvenire in utero durante una gravidanza o nei primi giorni di vita, il virus in tal caso può colpire le cellule cardiache (miociti) determinando una miocardite (infiammazione cardiaca) letale. Tale localizzazione, piuttosto comune alla fine degli anni 70’ e nei primi anni 80’, oggi è diventata estremamente rara; ciò è legato al fatto che praticamente tutte le cagne adulte sono vaccinate contro questo virus e possiedono quindi un certo grado di immunità nei confronti della malattia. I cuccioli, nelle prime settimane di vita, sono quindi protetti dall’immunità passiva materna; cioè è possibile poiché la madre, durante la gravidanza, passa ai cuccioli anticorpi contro il virus che permangono in circolo per circa 4 settimane dopo la nascita. Nelle settimane successive si verifica un calo degli anticorpi materni e i cuccioli diventano fortemente suscettibili all’infezione; inoltre, tale periodo di maggiore recettività coincide spesso con il momento della separazione dei cuccioli dalla madre, un fattore stressante che aumenta notevolmente il rischio di infezione. Per questo motivo, quando si adotta un cucciolo, è opportuno prestare molta attenzione a situazioni di possibile contagio (es. luoghi molto affollati con soggetti non vaccinati) e non bisogna mai sottovalutare la comparsa di sintomi quali anoressia, vomito e diarrea. Una volta avvenuto il contatto tra virus e cane si ha un periodo di incubazione che va dai 4 ai 14 giorni, dopo di che inizia la fase sintomatica. I sintomi possono essere molto diversi e dipendono dal grado di pericolosità della malattia (virulenza del virus), quantità di virus con cui il soggetto è venuto a contatto, difese immunitarie ed età del cane contagiato (più giovane è il cucciolo più pericoloso è la malattia).Figura 1: ciclo del parvovirus e strategie terapeutiche Sintomatologia I sintomi più comuni sono: anoressia febbre abbattimento del sensorio grave disidratazione vomito copioso che fatica a rispondere ai farmaci antiemetici grave diarrea liquida ed emorragica (l’aspetto delle feci viene anche definito a “marmellata di ciliegie”) I danni midollari causati dal virus portano a diminuzione dei globuli bianchi (neutropenia) che può predisporre a gravi infezioni batteriche secondarie. A livello intestinale il virus replica negli enterociti causando ulcerazioni molto gravi. Diagnosi I sintomi e la storia clinica (cucciolo non vaccinato che è stato a contatto con altri cani) fanno sospettare al veterinario questa malattia. Al fine di ottenere la conferma diagnostica il veterinario deve eseguire dei test specifici. Gli esami che vengono effettuati dal medico veterinario sono solitamente: esame emocromocitometrico esame biochimico completo emogasanalisi (eventuale) test per la ricerca del virus nelle feci (test ELISA o PCR) test sierologico per la ricerca di anticorpi nel sangue (eventuali) Terapia Confermata la diagnosi è importante iniziare tempestivamente la terapia ed è spesso necessario ospedalizzare i cani affetti da parvovirosi. Viene instaurata una fluidoterapia endovenosa continua, mirata a ristabilire l’idratazione e ripristinare gli elettroliti, ad esempio sodio e potassio, che sono stati persi con il vomito e con la diarrea. Spesso i cuccioli con parvovirosi sviluppano ipoglicemia e in tali casi la fluiditerapia viene integrata con soluzioni contenenti glucosio. Alla terapia fluida vengono solitamente associate altre terapie quali antibiotici, antiemetici, antiacidi, antidolorifici e albumine, cioè proteine che spesso vengono perse a causa dell’importante diarrea. Nei casi più gravi si deve ricorrere a trasfusioni di sangue. Poiché l’assunzione di alimento può peggiorare il problema vomito, in questi casi è consigliata la sospensione dell’alimentazione per bocca per passare eventualmente ad una nutrizione attraverso dei sondini per la nutrizione parenterale. Vista la contagiosità della malattia (potrebbe mettere in pericolo altri cani non vaccinati) e le cure necessarie, è evidente che si debba ricorrere all’ospedalizzazione in apposite strutture veterinarie che dispongano di reparti dedicati ad animali colpiti da malattie infettive (reparto infettivi). Generalmente il periodo di ricovero è di circa 7 – 10 giorni, ma per animali con sintomi lievi possono essere sufficienti 2-3 giorni. Un ottimo segno di ripresa è quando il cane ricomincia ad alimentarsi da solo senza vomitare. Vaccino e Prevenzione La parvovirosi può essere prevenuta con il vaccino. La prima somministrazione nei cuccioli può essere effettuata a 6-8 settimane di età e successivamente sono necessari dei richiami. Il vaccino viene ripetuto poi in età adulta. In generale esistono vaccini “core” ossia fortemente raccomandati, e vaccini “non core”, consigliati e che vengono generalmente somministrati in base allo stile di vita e all’ambiente in cui il cane vive. Quello per il parvovirus è un vaccino “core”, è quindi fortemente raccomandato per tutti i soggetti. È molto importante che i cani vengano vaccinati, sia per proteggere loro stessi sia per prevenire le infezioni di altri cuccioli. E’ importante adottare dei comportamenti adeguati quando si adotta un cucciolo;. In particolare va evitato il contatto tra cani non vaccinati, evitando le situazioni di maggiore affollamento e possibilmente, prima del completamento delle vaccinazioni, vanno evitati i parchetti frequentati da altri cani. In ambienti quali canili, rifugi, allevamenti, negozi di animali è necessario adottare misure preventive e nel caso in cui si individui un soggetto infetto, vanno adottate misure adeguate di disinfezione dell’ambiente per evitare la rapida diffusione del virus. Con la collaborazione della Dr.ssa Elena Zanato “DVM, Diplomato ECVIM-CA, EBVS® - European Veterinary Specialist in Small Animal Internal Medicine - Animali da compagnia, Endocrinologia non riproduttiva, medicina interna e terapia (Malattie Metaboliche).”Prof. Federico FracassiAutore #sppb-addon-1719818877863 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877863 img{}#sppb-addon-1719818877864 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877864 img{}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}
Che cos’è l’epatite cronica del cane? L’epatite cronica del cane è una malattia di natura infiammatoria e degenerativa a carico del fegato caratterizzata da una insorgenza lenta e da un andamento cronico e progressivo. Quando si parla di epatite cronica una distinzione fondamentale va fatta tra l’epatite cronica primaria, di cui parleremo in questo articolo, e quella secondaria. Nell’epatite cronica primaria il meccanismo patologico origina nel fegato e lo coinvolge direttamente causando delle alterazioni significative. Nell’epatite cronica secondaria invece, il processo patologico scatenante origina al di fuori del fegato (ad esempio nell’intestino, nel pancreas o nel cavo orale) con coinvolgimento solo susseguente del fegato e con comparsa di alterazioni lievi e poco significative. Questa forma viene chiamata anche epatite cronica reattiva a significare la reazione del fegato a un processo patologico insorto altrove. La prevalenza dell’epatite cronica primaria del cane è largamente sconosciuta. Tuttavia, si sospetta che la malattia sia sotto-diagnosticata per la scarsa propensione a eseguire biopsie del fegato necessarie al raggiungimento della diagnosi e per via della sua subdola insorgenza e lenta progressione che la rendono difficilmente sospettabile. Cosa causa l’epatite cronica nel cane? La vera causa dell’epatite cronica primaria del cane è in buona parte sconosciuta ma si sospetta che la malattia sia dovuta a una aberrante attivazione del sistema immunitario del cane nei confronti di componenti cellulari del fegato con successivo instaurarsi di un processo infiammatorio auto-propagante che a sua volta porta all’instaurarsi di danni strutturali irreversibili (malattia su base immunomediata). Diverse cause potenziali in grado di causare questa disfunzione del sistema immunitario sono state considerate dai ricercatori. Tra le più studiate si annoverano: - Malattie infettive - Malattie metaboliche - Farmaci e tossine ambientali Nonostante diversi studi, l’associazione tra queste cause e l’epatite cronica primaria del cane non è stata dimostrata in maniera convincente e la vera causa della malattia rimane elusiva. In alternativa alla disfunzione del sistema immunitario, un’altra causa di epatite cronica primaria del cane è rappresentata dall’accumulo eccessivo di rame all’interno del fegato (epatite cronica rame associata). In condizioni naturali il rame assunto con la dieta viene assorbito a livello intestinale e arriva al fegato dove viene utilizzato per catalizzare reazioni cellulari essenziali, viene immagazzinato come riserva e la quantità in eccesso viene eliminata attraverso le vie biliari e quindi attraverso l’intestino. In alcuni casi a causa di un difettoso meccanismo di trasporto e/o escrezione del rame, questo metallo pesante si accumula in maniera eccessiva nel fegato dove causa un grave e progressivo danno ossidativo con morte (apoptosi) delle cellule epatiche e una risposta infiammatoria secondaria massiccia.In questo caso è l’accumulo di rame a scatenare il processo infiammatorio (accumulo di rame primario). E’ tuttavia possibile che in alcuni casi di epatite cronica su base immunomediata, l’accumulo di rame avvenga secondariamente alla perdita di funzione delle cellule del fegato causata dal processo infiammatorio (accumulo di rame secondario). La distinzione tra queste due forme di accumulo di rame sarà fondamentale ai fini della scelta della terapia più adeguata e potrà avvenire solo mediante la misurazione effettiva della quantità di rame presente nella biopsia epatica. Quali razze di cane sono a maggior rischio di sviluppare l’epatite cronica? Premesso che l’epatite cronica (sia la forma immunomediata che quella rame-associata) può colpire cani di qualsiasi razza, sesso ed età, diversi studi scientifici hanno evidenziato delle predisposizioni di razza per entrambe le forme di epatite cronica del cane. Le razze maggiormente a rischio includono (lista non esaustiva): Dalmata (forma rame-associata) Labrador Retriever (forma immunomediata e forma rame-associata) Doberman Pinscher (forma immunomediata e forma rame-associata) West Highland White Terrier (forma rame-associata) Bedlington Terrier (forma rame-associata su base genetica) English e American Cocker Spaniel (forma immunomediata) English Springer Spaniel (forma immunomediata) L’età media dei cani con epatite cronica è intorno ai 7 anni tuttavia la malattia può colpire anche cani più giovani o anziani. Alcuni studi hanno inoltre riscontrato una maggior rischio di sviluppare la malattia per i cani di sesso femminile soprattutto per le razze Labrador Retriever, Doberman, Dalmata e English Springer Spaniel. Altri studi invece hanno riscontrato un rischio maggiore nei maschi di razza American e English Cocker Spaniel. Come si può sospettare clinicamente l’epatite cronica in un cane? Per via della grossa riserva funzionale del fegato e per via della natura insidiosa della malattia, l’epatite cronica può svilupparsi senza mostrare alcun sintomo clinico se non quando il problema è già avanzato.E’ importante quindi sospettare la malattia nei cani di razze a rischio anche in presenza di sintomi clinici aspecifici o lievi. I sintomi clinici più frequentemente notati dai proprietari di cani con epatite cronica sono i seguenti (tra parentesi è riportata la relativa percentuale di frequenza): Riduzione dell’appetito 61% Letargia/depressione 56% Colorazione giallastra di occhi, mucose orali e cute 34% Distensione addominale da liquido 32% Aumento della sete e dell’urinazione (polidipsia/poliuria) 30% Vomito 24% Diarrea 20% Sintomi neurologici (encefalopatia epatica) 7% Come già accennato, l’epatite cronica primaria del cane ha una fase sub-clinica o pre-clinica molto lunga durante la quale i sintomi clinici sono assenti o lievi, il che complica la diagnosi e la terapia tempestiva della malattia prima che si sviluppino gravi alterazioni (alcune irreversibili) del fegato. Fortunatamente, un aiuto dal punto di vista diagnostico ci viene fornito dagli esami di laboratorio, in particolare dal profilo biochimico. Come posso sospettare l’epatite cronica del cane con gli esami di laboratorio? Le indagini di laboratorio sono utili per avanzare un sospetto di epatite cronica (soprattutto le forme avanzate) ma non sono utili ad escludere la presenza della malattia perché possono risultare nella norma nonostante la malattia (seppur in forma lieve sia già presente). L’esame di laboratorio più utile per avanzare il sospetto di epatite cronica è il profilo biochimico. In particolare, l‘aumento significativo (> 2 volte il range superiore di laboratorio) e persistente (di durata > 2 mesi) dell’enzima ALT è fortemente indicativo di un danno significativo alle cellule epatiche e, se sono state escluse cause extra-epatiche dell’alterazione, renderebbe necessaria l’esecuzione di una biopsia epatica per escludere la presenza di epatite cronica. Altre alterazioni del profilo biochimico riportate in corso di epatite cronica del cane includono un aumento (inferiore in proporzione a quello della ALT) di altri enzimi del fegato come la ALP, la GGT e la AST, l’aumento della bilirubina (iperbilirubinemia) o, nei casi avanzati con insufficienza epatica, la diminuzione del glucosio (ipoglicemia), del colesterolo (ipocolesterolemia), delle albumine (ipoalbuminemia) e della BUN. Talvolta, soprattutto negli stadi terminali della malattia (cirrosi), gli enzimi epatici possono risultare nella norma o al di sotto dei range di riferimento per la perdita di massa vitale del fegato. L’ecografia addominale è utile per sospettare l’epatite cronica del cane? L’esame ecografico è generalmente molto utile per la valutazione d’insieme del fegato (della sua forma, dimensione e ecostruttura), delle vie biliari e delle strutture vascolari associate al fegato. Purtroppo la sua utilità nella diagnosi dell’epatite cronica è relativamente bassa in quanto in buona parte dei casi il fegato può apparire ecograficamente normale nonostante la presenza di gravi alterazioni del profilo biochimico. Si parla quindi di una bassa sensibilità dell’ecografia per la diagnosi di epatite cronica ovvero non si può escludere la malattia sulla base di un esame ecografico nella norma.In casi avanzati di epatite cronica il fegato potrebbe apparire ridotto di dimensioni (microepatica) con architettura gravemente distorta e si potrebbe riscontrare la presenza di liquido libero in addome (ascite) o la proliferazione di piccoli vasi sanguigni (shunt portosistemici acquisiti).Ecografia addominale di un cane con epatite cronica di stadio avanzato. Il fegato (F) appare gravemente ridotto di dimensioni, con perdita della normale apparenza ecografica e comparsa di una struttura diffusamente disomogenea. Cosa serve per confermare la diagnosi di epatite cronica del cane? Per confermare la diagnosi di epatite cronica sarà obbligatoria l’esecuzione di una biopsia epatica e la successiva richiesta dell’esame istologico che dovrà essere interpretato da un patologo esperto di malattie del fegato. Unitamente all’esame istologico della biopsia epatica è consigliato eseguire sempre un esame colturale della bile e delle colorazioni speciali per valutare l’accumulo di rame o pigmenti all’interno delle cellule del fegato. Quali sono i criteri istologici per la diagnosi di epatite cronica del cane? I criteri istologici tipici dell’epatite cronica includono la presenza di un infiltrato infiammatorio di tipo mononucleare (rappresentato da linfociti, plasmacellule e macrofagi) o misto (con presenza anche di cellule multinucleate) a distribuzione variabile nel contesto lobulo epatico (l’unità anatomica e funzionale del fegato), in associazione a morte degli epatociti (necrosi e apoptosi).In casi avanzati ci sarà presenza di fibrosi più o meno grave con la proliferazione dei piccoli dotti biliari e la formazione di isolotti di tessuto epatico circondato da fasci di collagene (rigenerazione nodulare).Nei casi molto avanzati la normale architettura del fegato sarà distorta e si parlerà di cirrosi epatica, che rappresenta lo stadio finale della malattia associato a una prognosi infausta. Al fine di escludere la presenza di un accumulo eccessivo di rame come causa della epatite cronica sarà necessario eseguire una colorazione speciale sul tessuto epatico (con rodanina) che permetterà di notare la presenza e la distribuzione di rame nel campione bioptico e in ultima analisi la quantificazione del rame (espressa in mg/kg di sostanza secca) sul tessuto.In caso di una concentrazione di rame > 700 mg/kg ma < 1500 mg/kg si tratterà di un accumulo di rame secondario alla infiammazione (epatite cronica immunomediata).Nel caso invece di una quantità > 1500 mg/kg si tratterà di un accumulo primario di rame con infiammazione secondaria (epatite cronica rame-associata).Immagine istologica di una biopsia epatica sottoposta a colorazione con rodanina. Si apprezza una area del lobulo epatico con (*) con intensa colorazione rossastra indicativa di accumulo eccessivo di rame e di epatite cronica rame-associata. Quale terapia per l’Epatite Cronica nel cane? Il veterinario, in aggiunta alla terapia sintomatica (basata sul controllo dei sintomi e delle complicazioni derivate dalla malattia), opterà per la terapia dell’epatite cronica del cane appropriata in base al tipo di patologia: immunomediata o rame-associata. Nel caso della epatite cronica Immunomediata la terapia si basa sull’utilizzo di farmaci immunosoppressori in aggiunta a farmaci di supporto come antiossidanti, dieta con bassissima quantità di rame e proteine di alto valore biologico. Solitamente la terapia sarà necessaria per almeno 12 mesi con tentativi di ridurre il dosaggio del farmaco in base alla risposta clinica e al miglioramento della concentrazione ematica di ALT. Tuttavia in alcuni casi il cane andrà trattato indefinitamente. Nella epatite cronica rame-associata: bisognerà utilizzare farmaci cosiddetti “chelanti del rame” (come la D-penicillamina) che agiscono riducendo l’assorbimento intestinale del rame e favorendo l’eliminazione del rame accumulato a livello epatico, in aggiunta a farmaci antiossidanti e dieta a basso contenuto di rame. Solitamente saranno necessari 6-9 mesi di terapia per riuscire a ridurre in maniera efficace la quantità di rame accumulata in eccesso nel fegato. Per monitorare la risposta alla terapia sarebbe ideale ripetere la biopsia epatica e quantificazione del rame, ma spesso si preferisce monitorare i sintomi clinici e l’andamento della concentrazione ematica della ALT come indici indiretti di remissione. Qual è la prognosi dell’epatite cronica del cane? La prognosi nella epatite cronica del cane dipenderà dallo stadio della malattia e dalla tempestività della diagnosi e dell’inizio della terapia. Tra i fattori prognostici negativi ci sono: Riscontro di iperbilirubinemia al profilo biochimico La presenza di ascite all’esame ecografico (associata a fibrosi e ipertensione portale) Gravità ed estensione della fibrosi all’esame istologico “Med. Vet., Diplomato ACVIM, Diplomato ECVIM-CA, MRCVS, EBVS® - Specialist in Small Animal Internal Medicine”Dr. Fabio ProcoliAutore #sppb-addon-1719818877863 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877863 img{}#sppb-addon-1719818877864 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877864 img{}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}

Con il termine di pancreatite si definisce l’infiammazione del pancreas. Il pancreas è un organo ghiandolare localizzato nell’addome craniale, adiacente al piccolo intestino. In condizioni di normalità (fisiologiche), il pancreas svolge due funzioni molto importanti. Attraverso la produzione di insulina regola il metabolismo del glucosio e grazie alla secrezione di enzimi quali proteasi, amilasi, lipasi e fosfolipasi e tripsina (successivamente convertita a tripsinogeno) prende parte ai processi digestivi degli alimenti.Da questo si deduce che una patologia legata ad un’infiammazione di quest’organo può causare conseguenze gravi per l’organismo.La pancreatite acuta nel cane ad oggi è una patologia estremamente temuta perché può manifestarsi in modo grave ed avere un alto tasso di mortalità e tempi di guarigione molto lunghi. Esistono tuttavia vari gradi di gravità e alcune forme sono lievi e possono addirittura passare inosservate e senza sintomatologia evidente. I cani affetti da questa patologia necessitano solitamente di varie terapie che generalmente richiedono il ricovero.Vengono colpiti cani di media età ma può insorgere anche in soggetti più giovani e potenzialmente a qualunque età.Le cause di pancreatite acuta nel cane non sono ben chiare ma sono stati individuati diversi fattori predisponenti. Sicuramente una dieta ricca di grassi e povera in proteine può predisporre a questo tipo di patologia, anche l’eccessiva integrazione con alimenti non dedicati esclusivamente al cane (ad esempio cibo per gatti), o l’ingestione di alimenti avariati (ingestione di rifiuti) possono essere nocivi. Altri fattori che possono indurre la pancreatite sono l’ipercalcemia, l’ipertrigliceridemia, l’obesità, infiammazioni concomitanti quali enteriti, colangiti (ossia infiammazioni alla cistifellea), colangioepatiti (ossia infezioni alle vie biliari e al fegato) e l’assunzione di determinati tipi di farmaci quali ad esempio l’aziatioprina (farmaco immunosoppressivo), il bromuro di potassio (farmaco per l’epilessia) i sulfamidici (antibiotici), il cisplatino e l’asparginasi (farmaci oncologici).Potenzialmente anche alcuni farmaci possono predisporre allo sviluppo di pancreatite. Un tempo si credeva che anche le terapie cortisoniche potessero predisporre alla pancreatite ma questo non è stato confermato da recenti studi.Esiste anche una predisposizione di razza, e le cinque razze in cui è stata osservata una maggiore prevalenza della patologia sono il Miniature Schnauzer, lo Shetland Sheepdog, lo Yorkshire Terrier, il Barbone Nano e il Bichon Frisè. Va tuttavia ricordato che la pancreatite acuta può insorgere in qualunque razza.Anche cause traumatiche, sia chirurgiche che accidentali (es. grossi traumatismi addominali), possono predisporre all’insorgere della pancreatite acuta. A volte, l’ipoperfusione del pancreas in seguito a procedure anestesiologiche può predisporre allo sviluppo di pancreatite.Cani con altre patologie concomitanti, ad esempio disturbi endocrini (es. morbo di Cushing, ipotiroidismo, diabete mellito) sono maggiormente predisposti allo sviluppo di pancreatite.Sono stati identificati anche dei fattori ereditari, più precisamente mutazioni della tripsina che predispongono allo sviluppo dell’infiammazione del pancreas. Nella figura 1 vengono riportate le principali cause di pancreatite acuta nel cane. Indipendentemente dalla causa che raramente viene identificata con certezza, il decorso fisiopatologico di questa malattia è ben chiaro: uno o più dei fattori predisponenti sopracitati causa un rilascio eccessivo di enzimi pancreatici in particolare del tripsinogeno attivato a tripsina che innesca un processo di autodigestione dell’organo e un’intensa e acuta cascata infiammatoria. Figura 1: Schematizzazione dei fattori in grado di causare la pancreatite acuta nel cane. Tratto da Petrelli A, Fracassi F: La pancreatite acuta nel cane: eziopatogenesi, sintomatologia e diagnosi. Veterinaria 2016; 30:99-114Quali sintomi può dare questa patologia?Come detto in precedenza questa non è una malattia da sottovalutare e non sono da trascurare neanche i sintomi che possono variare da molto lievi, come ad esempio disappetenza, qualche sporadico episodio di vomito o lieve fastidio addominale, fino al vero e proprio addome acuto (addome estremamente dolente) con vomito frequente (vari episodi al giorno), anoressia e il così detto “atteggiamento a preghiera”( zampe anteriori allungate sul pavimento e zampe posteriori estese), disidratazione fino ad arrivare a stati di shock in cui il cane non riesce a stare in piedi.Figura 2. Cane con pancreatite acuta e assume il così detto “atteggiamento a preghiera” Questi sintomi (Tabella 1) non sono tuttavia patognomonici di pancreatite acuta, cioè fanno sospettare questa patologia come tante altre del comparto craniale addominale quali ad esempio problematiche epatiche, di cistifellea, gastriche o duodenali. Sintomi % Anoressia 91% Vomito 90% Debolezza 79% Dolore Addominale 58% Disidratazione 33% Febbre 23% Tabella 1: Sintomi con relative frequenze in corso di pancreatite acuta nel cane. Come si diagnostica questa patologia?La diagnosi si effettua integrando i dati dell’anamnesi (ossia la storia dell’animale), della visita clinica, degli esami di laboratorio e di diagnostica per immagini (soprattutto l’ecografia). Gli esami emato-biochimici e delle urine non permettono di individuare elementi specifici per diagnosticare la pancreatite; tuttavia, sono necessari per escludere le altre diagnosi differenziali che possono determinare una sintomatologia simile. A tele proposito gli esami di base che devono essere eseguiti sono:- Esame emocromocitometrico completo- Esame biochimico completo- Esame delle urineEsistono poi dei test più specifici per individuare la pancreatite:- Misurazione della lipasi e/o della così detta lipasi DGGR- Test per l’immunoreattività della lipasi pancreatica canina (cPLI)- Test per l’immunoreattività tripsinosimile sierica (TLI)La lipasi DGGR e il cPLI, pur con vari limiti (nessun test è perfetto), sono considerati i due parametri più attendibili per la diagnosi di pancreatite acuta nel cane. Va tuttavia sottolineato che per qualunque parametro laboratoristico esistono false positività (ossia il test è positivo ma la malattia non è presente) e false negatività (il test è negativo ma la malattia è presente). E’ compito del veterinario quello di integrare tutte le informazioni per emettere una diagnosi, non è possibile infatti basarsi su un singolo test. Ecografia addominale: I segni evidenziabili ecograficamente sono in relazione alla gravità della patologia, alla durata e all’estensione dell’infiammazione del tessuto pancreatico e delle strutture circostanti. Secondo uno studio, la capacità dell’ecografia addominale di evidenziare la pancreatite acuta nel cane è del 68%.Come si cura la pancreatite acuta nel cane ?Al pari di quanto avviene per molte patologie, la terapia dovrebbe essere finalizzata alla rimozione dell’eventuale causa sottostante. Per tale motivo risulta di fondamentale importanza indagare la presenza di potenziali fattori di rischio quali la presenza di ipertrigliceridemia, ipercalcemia, ingestione di rifiuti, tossici o alimenti fortemente ricchi di lipidi, anestesie recenti o somministrazione di farmaci. Nel caso in cui l’animale risulti in terapia con farmaci in grado di indurre pancreatite, quando possibile, tali farmaci andrebbero sospesi o quantomeno sostituiti. Purtroppo molto spesso non è possibile identificare la causa scatenante.Le terapie e la prognosi dipendono molto dallo stato di gravità della pancratite.Una grave pancreatite acuta nel cane è una patologia molto seria con alto tasso di mortalità e richiede cure intensive mentre una pancreatite moderata può essere gestita con fluidoterapia endovenosa e analgesici e i pazienti con pancreatite molto lievi possono a volte, anche se raramente, essere gestiti con terapie domiciliari.Esistono forme estremamente mortali di pancreatite acuta, le pancreatiti necrotizzanti gravi.Terapia di supportoUn’adeguata fluidoterapia rappresenta il punto cardine nella terapia della pancreatite acuta. La fluidoterapia deve essere individualizzata secondo le esigenze del singolo paziente.AlimentazioneFino a poco tempo fa l’indicazione era quella di non alimentare l’animale per diversi giorni al fine di “far riposare” il pancreas. Non esiste evidenza scientifica che questo sia corretto e pertanto le indicazioni sono quelle di alimentare da subito i soggetti con pancreatite. L’unica controindicazione è rappresentata dai cani con vomito frequente e difficile da bloccare; tuttavia, dopo 12 ore di assenza di vomito è indicato iniziare ad alimentare il soggetto con un alimento a bassissimo tenore lipidico. Nei casi di anoressia prolungata (2-4 giorni) è indicata una nutrizione enterale (sondino nasale, esofageo o gastrico). AnalgesiaNell’uomo la dolorabilità addominale viene riportata nel 90% dei soggetti con pancreatite. Nei nostri animali vengono indicate percentuali più basse. Nei nostri animali questi dati sono molto probabilmente falsati dal fatto che non siamo in grado di discriminare se vi sia o meno dolore addominale e molto probabilmente queste percentuali sono più alte. E’ opportuno considerare che ciascun cane e gatto con pancreatite abbia dolore addominale e dovrebbe essere trattato di conseguenza. Possono essere utilizzati differenti protocolli di analgesia ma è bene che i farmaci antinfiammatori vengano evitati.AntiemeticiNel caso in cui il cane, nonostante la terapia fluida e l’eventuale gastroprotettore, continui a vomitare è opportuno somministrare un antiemetico. Somministrazione di plasmaIl plasma contiene numerose sostanze quali fattori della coagulazione, inibitori delle proteasi albumina che possono essere benefici in un soggetto con pancreatite. Nonostante la somministrazione di plasma venga suggerita da molti autori né in medicina umana né in medicina veterinaria è stato provato che la terapia abbia un’influenza sulla prognosi dei pazienti con pancreatite acuta. AntibioticiRaramente i cani con pancreatite presentano complicazioni infettive e pertanto non vi è evidenza che la terapia antibiotica sia utile nel management di questa patologia. La terapia antibiotica può eventualmente risultare utile nelle forme più gravi al fine di evitare una traslocazione batterica dall’intestino. AntinfiammatoriNon vi è indicazione che vi siano dei benefici riguardanti l’utilizzo di corticosteroidi o antinfiammatori non steroidei (FANS) nella terapia della pancreatite. Molti FANS sono stati inoltre riconosciuti come possibile causa di pancreatite e vanno pertanto evitati.Intervento chirurgicoNumerosi protocolli chirurgici sono stati proposti nella gestione della pancreatite acuta e cronica quali il lavaggio peritoneale, la pancrectomia parziale e la necrosectomia. Non esistono studi sistematici che dimostrino l’efficacia di tali procedure nel cane. Attualmente le eventuali indicazioni chirurgiche riguardano soltanto gli ascessi pancreatici o le pseudo cisti che non tendono a regredire.Con la collaborazione della Dr.ssa Elena Zanato “DVM, Diplomato ECVIM-CA, EBVS® - European Veterinary Specialist in Small Animal Internal Medicine - Animali da compagnia, Endocrinologia non riproduttiva, medicina interna e terapia (Malattie Metaboliche).”Prof. Federico FracassiAutore #sppb-addon-1719818877863 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877863 img{}#sppb-addon-1719818877864 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877864 img{}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}
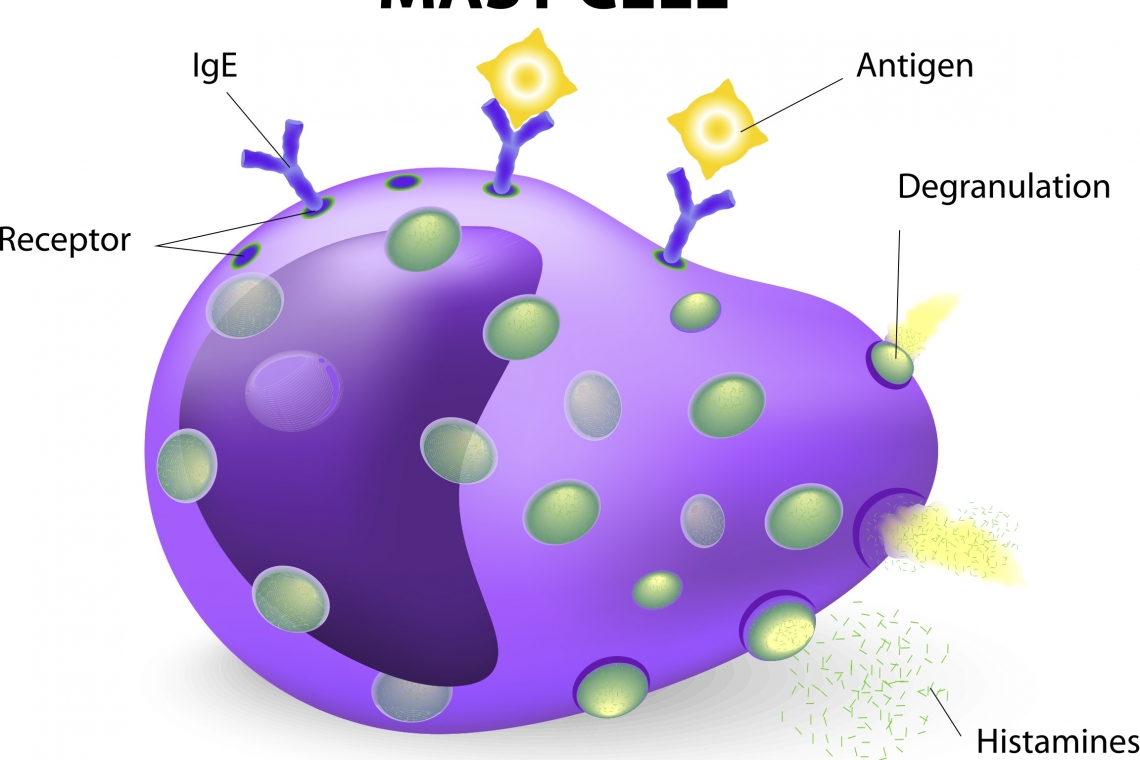
Il mastocitoma del cane è una neoplasia maligna della cute molto comune nel cane. I mastociti sono cellule che intervengono nelle allergie ed infiammazione. I granuli contenuti al loro interno possono essere rilasciati in grandi quantità (degranulazione), e provocare alterazioni locali (prurito, eritema, ulcerazione) e sistemiche (ulcere gastriche, emorragie, ipotensione). Alcune razze di cani sono maggiormente predisposte al mastocitoma, tra queste il boxer, carlini, bulldog, boston terrier, labrador retriever, golden retriever, weimaraner, rhodesian ridgeback, beagle, shar-pei, stafforshire terrier, ma di fatto il mastocitoma del cane può interessare qualunque razza. La causa è sconosciuta, ma si ipotizzano la predisposizione genetica in alcune razze, le anormalità molecolari, e l’infiammazione cronica. Solitamente il cane viene portato dal veterinario per la presenza di un nodulo cutaneo, che può o meno essere ulcerato in superficie e alopecico, e che può aver alternato periodi di scomparsa a periodi di recrudescenza. Questo è dovuto al rilascio di istamina da parte del tumore, che provoca un rigonfiamento del nodulo. Alcuni mastocitomi nel cane hanno un comportamento indolente, e possono essere presenti anche da anni, altri sono più aggressivi, e metastatizzano velocemente, prima ai linfonodi regionali, poi ai visceri (soprattutto fegato e milza). Diagnosi Il primo passo nell’iter diagnostico è la citologia del nodulo. Una volta confermato citologicamente che si tratta di un mastocitoma, il tumore deve essere stadiato, per verificare se ci sono o meno metastasi. La stadiazione serve per scegliere le opzioni terapeutiche migliori e per definire la prognosi. Il linfonodo sentinella, identificato mediante diagnostica per immagini avanzata, deve essere valutato mediante ago aspirato; sono necessarie le radiografie del torace, soprattutto per escludere altri problemi subclinici, l’ecografia addominale e la citologia di fegato e milza. In alcuni casi è necessario valutare anche il midollo osseo. Gli esami del sangue di base, insieme al profilo coagulativo e all’esame delle urine, completano la fase di stadiazione, e permettono di ottenere informazioni circa lo stato generale di salute del cane. Terapia La chirurgia rappresenta la terapia d’elezione per la maggior parte dei mastocitomi che non hanno metastatizzato, o che hanno metastatizzato al linfonodo regionale. Oltre alla rimozione del tumore primitivo è utile asportare sempre anche il linfonodo sentinella, indipendentemente dal risultato della citologia. L’esame istopatologico del tumore primitivo e del linfonodo sentinella permette di fornire moltissime informazioni prognostiche ed è uno tra i fattori prognostici più importanti, insieme alla stadiazione. In alcuni casi vengono suggeriti ulteriori approfondimenti, che permettono di anticipare meglio il comportamento biologico. In altri casi (grado istologico elevato, presenza di metastasi), la chirurgia non è sufficiente, e sarà necessario ricorrere alla terapia medica, che consiste in chemioterapia tradizionale o farmaci a bersaglio. In particolare, per questi ultimi, è consigliato richiedere sul tumore primitivo l’analisi mutazionale, dal momento che i farmaci inibitori tirosin-chinasici funzionano meglio o esclusivamente in caso di mutazione di un gene: il gene c-kit. La radioterapia può essere un’opzione se il tumore non può essere rimosso chirurgicamente, oppure se non si è ottenuto il controllo locale. I mastocitomi sono, infatti, radiosensibili, e la radioterapia può essere presa in considerazione in un approccio multimodale. Prognosi La prognosi varia moltissimo in funzione di grado istologico del tumore primitivo, stato del linfonodo sentinella e risultato della stadiazione del paziente. Numerosi altri fattori prognostici sono stati ben documentati e dovranno essere valutati in concerto, tra cui segnalamento, sede di insorgenza, presenza di ulcerazione e dimensione del mastocitoma primitivo, stato mutazionale di c-kit, Ki67 e KIT pattern. Per questi motivi il veterinario potrà proporre numerosi e utilissimi approfondimenti diagnostici in caso di diagnosi di mastocitoma del cane. “Med. Vet., Professore Associato Dipartimento di Scienze Mediche Veterinarie Alma Mater Studiorum, Università di Bologna, Diplomata ECVIM-CA, EBVS® - European Veterinary Specialist in Small Animal Oncology - Animali da compagnia - (Oncologia)”Prof.ssa Laura MarconatoAutore #sppb-addon-1719818877863 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877863 img{}#sppb-addon-1719818877864 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877864 img{}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}

Il mastocitoma del gatto è una neoplasia maligna che origina dai mastociti. I mastociti sono cellule che intervengono nelle allergie ed infiammazione. I granuli contenuti al loro interno possono essere rilasciati in grandi quantità (degranulazione), e provocare alterazioni locali (prurito, eritema, ulcerazione) e sistemiche (ulcere gastriche, emorragie, ipotensione). Nel gatto sono descritte due forme di mastocitoma: la cutanea e la forma viscerale. La forma cutanea è spesso localizzata e curabile con la chirurgia. Solitamente il gatto viene portato dal veterinario per la presenza di un nodulo cutaneo, che può o meno essere ulcerato in superficie e alopecico e che può aver alternato periodi di scomparsa a periodi di recrudescenza. Questo è dovuto al rilascio di istamina da parte del tumore, che provoca un rigonfiamento del nodulo. A volte, però, i noduli cutanei rappresentano una forma metastatica di mastocitoma che ha preso origine dalla milza o dall’intestino. In queste forme di mastocitoma viscerale, il gatto manifesta sintomi vaghi, tra cui inappetenza, vomito e perdita di peso. Il primo passo nell’iter diagnostico è la citologia del nodulo. Una volta confermato che si tratta di un mastocitoma, il tumore anche in questo caso deve essere stadiato. La stadiazione serve per scegliere le opzioni terapeutiche migliori e per definire la prognosi. Il linfonodo regionale deve essere valutato mediante ago aspirato; sono necessarie le radiografie del torace, l’ecografia addominale e la citologia di fegato, milza e di qualunque lesione venga visualizzata. Completano la fase di stadiazione gli esami del sangue di base, insieme al profilo coagulativo ed all’esame delle urine. Tutti questi esami permettono di ottenere informazioni circa lo stato generale di salute del gatto. La chirurgia rappresenta la terapia d’elezione per la maggior parte dei mastocitomi cutanei. In caso di mastocitoma viscerale, splenico o intestinale, deve essere presa in considerazione la terapia chirurgica. In funzione dell’esito della stadiazione e di altri parametri prognostici, può essere introdotta la terapia medica. La radioterapia non è quasi mai presa in considerazione.Quindi se il vostro gatto presenta un nodulo cutaneo oppure se mostra sintomi vaghi di inappentenza, perdita di peso o vomito il consiglio è di recarvi subito dal vostro veterinario per effettuare tutti gli esami diagnostici necessari. “Med. Vet., Professore Associato Dipartimento di Scienze Mediche Veterinarie Alma Mater Studiorum, Università di Bologna, Diplomata ECVIM-CA, EBVS® - European Veterinary Specialist in Small Animal Oncology - Animali da compagnia - (Oncologia)”Prof.ssa Laura MarconatoAutore #sppb-addon-1719818877863 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877863 img{}#sppb-addon-1719818877864 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877864 img{}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}

Il linfoma del cane è una neoplasia maligna spontanea che assomiglia al linfoma non-Hodgkin dell’uomo. Rappresenta il 7-24% di tutti i tumori maligni del cane. La causa è sconosciuta; si ipotizzano predisposizione genetica, esposizione ad inquinanti ambientali, ed aberrazioni cromosomiche. Da un punto di vista anatomico, esistono diverse forme, tra le quali la multicentrica è la più comune. Tutte le forme anatomiche possono coinvolgere il sangue e/o il midollo osseo (fase leucemica). I sintomi solitamente sono aspecifici, e sono da ricondurre agli organi colpiti. Solitamente il primo segno clinico è dato dall’aumento di volume dei linfonodi periferici. La diagnosi richiede vari esami, che permettono anche di accertare l’estensione del coinvolgimento tumorale (stadio clinico). L’ago aspirato di un linfonodo periferico permette di formulare il sospetto di linfoma, che andrà poi confermato mediante fenotipizzazione, tecnica utile anche per definire se il linfoma ha preso origine dalle cellule B o T. Per accertare lo stadio clinico, è necessario eseguire le radiografie del torace, l’ecografia addominale, la valutazione citologica di fegato e milza, e del sangue midollare. Nel cane, così come nell’uomo, esistono molti tipi di linfoma, la cui prognosi e terapia si differenziano notevolmente. Per conoscere l’esatto tipo di linfoma, è necessario rimuovere chirurgicamente un linfonodo periferico e sottoporlo ad analisi istologica ed immunoistochimica (marcatori). La chemioterapia rappresenta la terapia d’elezione, perché i chemioterapici, una volta somministrati, circolano per tutto l’organismo e hanno la possibilità di venire in contatto con le cellule tumorali. La chirurgia e la radioterapia hanno un’applicazione terapeutica ridotta, perché attaccano le cellule tumorali in un solo sito. Lo scopo della chemioterapia nei pazienti malati di linfoma è di indurre una “remissione completa”.Per “remissione” s’intende la scomparsa temporanea di tutti i sintomi. Gli animali con linfoma in remissione completa appaiono normali e conducono una vita perfettamente normale. Tuttavia una piccola percentuale di cellule tumorali sopravvive, e può ad un certo punto proliferare di nuovo, rendendo evidente la sintomatologia. Si parla in questo caso di “recidiva”, e l’animale non è più in remissione. Esistono diversi chemioterapici che possono essere utilizzati per uccidere le cellule tumorali, e molto spesso è preferibile usare una combinazione di tali farmaci per aumentare l’efficacia. La chemioterapia in corso di linfoma ha lo scopo di garantire una buona qualità di vita, prolungando la sopravvivenza. Un animale non trattato sopravvive in genere 4-6 settimane dalla diagnosi. La chemioterapia è molto ben tollerata dalla maggior parte degli animali; in alcuni casi tuttavia possono insorgere effetti collaterali, che richiedono una modificazione del protocollo.La chemioterapia non cura cani e gatti malati di linfoma, ma nella maggior parte dei casi migliora la quantità e la qualità di vita. Oggi è possibile per alcuni linfomi abbinare l’immunoterapia (vaccino terapeutico) alla chemioterapia. Non tutti i cani sono candidati: l’iter diagnostico permette di definire alcuni parametri utili ai fini della scelta terapeutica. “Med. Vet., Professore Associato Dipartimento di Scienze Mediche Veterinarie Alma Mater Studiorum, Università di Bologna, Diplomata ECVIM-CA, EBVS® - European Veterinary Specialist in Small Animal Oncology - Animali da compagnia - (Oncologia)”Prof.ssa Laura MarconatoAutore #sppb-addon-1719818877863 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877863 img{}#sppb-addon-1719818877864 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877864 img{}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}
L’eziologia dell’ipertiroidismo è complessa e multifattoriale; sono stati presi in causa fattori genetici, immunologici e nutrizionali senza tuttavia individuare il ruolo predominante di uno rispetto agli altri.Anche l’esposizione cronica a interferenti endocrini attraverso l’ambiente, la dieta o l’acqua potrebbe ricoprire un ruolo nella patogenesi dell’ipertiroidismo, così come dimostrato per le patologie tiroidee nell’uomo. Recenti studi hanno dimostrato la presenza di alti livelli nel siero di gatti, di un altro gruppo di contaminanti ambientali, i polibromodifenileteri (PBDE), anch’essi noti per le loro caratteristiche nocive. I polibromodifenileteri PBDE fanno parte dei ritardanti di fiamma e, come tali, in passato si ritrovavano in un’ampia gamma di prodotti (es: plastiche, articoli tessili e apparecchiature elettroniche). Tali molecole possono migrare e unirsi alla polvere dove raggiungono alte concentrazioni.I gatti domestici, considerate le loro abitudini, possono quindi venire in contatto con queste sostanze sia attraverso la via alimentare che tramite il grooming e, condividendo lo stesso ambiente dell’uomo, rappresentano l’animale sentinella per le contaminazioni ambientali domestiche.ASPETTI CLINICI E DIAGNOSTICI DELL’IPERTIROIDISMO FELINO Segnalamento: qual’è il paziente tipico ? Non vi sono predisposizioni di razza o sesso per lo sviluppo dell’ipertiroidismo, è stata tuttavia ipotizzata una sorta di “protezione genetica” poiché alcune razze di gatti, quali il Siamese e l’Himalayano, presentano un’incidenza minore della patologia.Nella maggior parte dei casi la diagnosi viene effettuata a 12-13 anni di età (range 4-22) e in meno del 5% dei soggetti è diagnosticato ad un’età inferiore ai 10 anni. In letteratura esiste solo un caso di ipertiroidismo giovanile dove la patologia è stata riscontrata in un gattino di 8 mesi.27 Sintomi più frequenti Si tratta di una patologia insidiosa e progressiva i cui effetti possono interessare tutto l’organismo o interessare un singolo apparato. La presentazione clinica e la gravità dei segni clinici sono variabili e dipendono dalle capacità di adattamento dell’organismo, dalla durata e dalla presenza o meno di patologie concomitanti. Il segno clinico principe è la perdita di peso, presente nel 90% circa dei soggetti, associata spesso ad aumento dell’appetito (polifagia). Entrambi questi sintomi sono legati ad un accelerato metabolismo dato dalla malattia. Il dimagrimento può essere più o meno marcato e può esitare in cachessia alla quale cui si può associare atrofia muscolare per un aumentato catabolismo proteico. Comunemente si osserva vomito ed occasionalmente diarrea (aumentata frequenza di defecazione, aumento di volume delle feci o steatorrea). L’aumento del transito gastrointestinale, l’aumentata ingestione di grassi dovuta alla polifagia e una minor efficienza del pancreas esocrino possono a volte portare a diarrea. In meno della metà dei soggetti è segnalata la presenza di poliuria/polidipsia (urina e beve maggiormente). In circa il 10% dei casi è possibile riscontrare quello che viene chiamato “ipertiroidismo apatico” dove aumento dell'appetito e iperattività sono sostituite da anoressia e depressione, permane invece il dimagrimento. L’ipertiroidismo può anche causare uno stato di ipertensione sistemica che può riflettersi a livello renale. Riepilogo dei principali sintomi dell’ipertiroidismo felino Dimagrimento 92% Polifagia (molto appetito) 55% Vomito 47% Iperattività 41% Poliuria e Polidipsia (urina e beve molto) 33% Inappetenza o anoressia 26% Debolezza muscolare e letargia 25% Diarrea 21% Dispnea (difficoltà nella respirazione) 11% Alterazioni del pelo \ Alopecia 7% Autore Peterson et al. (1983 - 2016) La visita clinica dal veterinarioAlla vista clinica effettuata dal Medico Veterinario, la maggior parte dei pazienti si presenta in condizioni nutrizionali scadenti, con mantello ispido, trasandato e possono essere presenti aree in cui manca il pelo. Gatto europeo maschio di 14 anni affetto da ipertiroidismo. Si noti lo scadente stato di nutrizione e lo scadente stato del mantello.Nel 90% dei casi è possibile apprezzare un nodulo tiroideo palpabile.In rari casi il nodulo può raggiungere notevoli dimensioni ed in questo caso è anche possibile che il nodulo non sia più benigno bensì maligno.Gatto Europeo in cui si evidenzia un nodulo tiroideo di grandi dimensioni dovuto a carcinoma tiroideo All’auscultazione è frequente evidenziare la presenza di tachicardia, soffio sistolico e, meno frequentemente, aritmie. La tachicardia (≥ 220 bpm), presente nel 30% dei gatti ipertiroidei, è dovuta ad un aumento del tono simpatico e ad una diminuzione del parasimpatico. Gli ormoni tiroidei attivano, inoltre, geni che codificano per proteine strutturali e regolatorie cardiache con conseguente aumento della contrattilità miocardica e sviluppo di cardiopatie. All’esame ecocardiografico è di comune riscontro la presenza di una cardiomiopatia ipertrofica che può portare ad insufficienza cardiaca e tromboembolismo aortico. Esami diagnostici Essendo l’ipertiroidismo una patologia geriatrica, è frequente la presenza di patologie concomitanti che possono complicarne il quadro clinico. Non esistono segni clinici patognomonici per l’ipertiroidismo, per tanto la diagnosi definitiva richiede la dimostrazione di un persistente aumento degli ormoni tiroidei in circolo. Il diagnostico differenziale di gatti con segni clinici compatibili con ipertiroidismo dovrebbe includere: diabete mellito, malassorbimento gastrointestinale o maldigestione (es. insufficienza pancreatica esocrina), neoplasie (es. linfoma del tratto gastroenterico), malattia renale cronica, parassiti, gravi errori alimentari. Test di screening Gli esami emato-biochimici di base e l’esame delle urine sono utili soprattutto per escludere altre patologie e in parte permettono di supportare la diagnosi. L’esame emocromocitometrico fornisce solitamente informazioni aspecifiche. É frequente il rinvenimento di un leucogramma da stress mentre è raro il riscontro di anemia. Al profilo biochimico il rilievo più caratteristico, presente nel 90% dei gatti, è l’aumento lieve-moderato di almeno uno degli enzimi epatici. Nel 75% dei gatti si osserva un aumento dell’ALT e della ALP. Un aumento marcato degli enzimi epatici potrebbe essere suggestivo di danno d’organo, tuttavia molti gatti ipertiroidei anche con un grave aumento di attività sierica degli enzimi epatici hanno una funzionalità epatica normale. Ulteriori approfondimenti per patologie epatobiliari trovano una giustificazione solamente in caso di mancato miglioramento dei valori epatici nei primi due mesi di terapia o qualora il paziente mostri ittero o disoressia/anoressia. Test di funzionalità tiroidea La diagnosi di ipertiroidismo è confermata con il riscontro di un aumento delle concentrazioni circolanti di ormoni tiroidei o con tecniche più sofisticate. A fini diagnostici ci si affida alla misurazione del T4 totale poiché la misurazione del T3 da luogo ad un 25-30% di falsi negativi. Per la diagnosi si può valutare anche il T4 libero (free T4 o fT4) che è tuttavia meno specifico rispetto al T4. Anche la misurazione del cTSH può aiutare nel definire la diagnosi di ipertiroidismo. La patologia non può essere esclusa dal solo ritrovamento di valori normali di T4, soprattutto nei gatti in cui la sintomatologia clinica e la presenza di un nodulo tiroideo risultino evidenti. In questi casi è consigliato ripetere le misurazioni del T4 dopo 2-4 settimane, in alternativa, soprattutto per i casi dubbi, è possibile effettuare una scintigrafia. In gatti anziani presentati per segni clinici compatibili con l’ipertiroidismo, confermare la diagnosi è abbastanza semplice, infatti, più del 90% presenta delle concentrazioni sieriche di T4 molto al di sopra del range di riferimento. La misurazione del T4 è relativamente economica e facilmente attuabile, per questi motivi è il test di scelta per lo screening di gatti con sospetto ipertiroidismo. Ecocardiografia Di comune riscontro all’esame ecocardiografico di gatti ipertiroidei è la presenza della cardiomiopatia ipertrofica che si evidenzia con ipertrofia del ventricolo sinistro, dilatazione di atrio e ventricolo sinistro e ipertrofia del setto interventricolare. Frequentemente si riscontra l’aumento della frazione di accorciamento, conseguente all’ipercontrattilità miocardica. Nei casi più avanzati la cardiomiopatia ipertrofica può portare ad insufficienza cardiaca e tromboembolismo aortico. Radiografia Più della metà dei gatti ipertiroidei mostra segni di cardiomegalia del settore sinistro che si associano a versamento pleurico ed edema polmonare in caso di insufficienza cardiaca. Ecografia dela tiroide L’ecografia della regione cervicale può essere usata per valutare la ghiandola tiroidea e fare una stima del suo volume. A differenza dell'uomo, l'ecografia tiroidea non è un esame routinariamente effettuato per la diagnosi di ipertiroidismo felino. I lobi tiroidei dei gatti con ipertiroidismo sono solitamente aumentati di dimensioni in modo uniforme e meno ecogeni rispetto ai lobi tiroidei normali e a volte possono essere identificate delle strutture cistiche all’interno della tiroide. Terapia Il Medico Veterinario deciderà l’approccio terapeutico più giusto per lo specifico paziente, le opzioni possono essere farmacologiche, radioterapiche o chirurgiche. Monitoraggio della terapia farmacologica Il paziente ipertiroideo in terapia farmacologica necessita di monitoraggio clinico e degli esami di laboratorio. Il primo controllo può essere effettuato a 2-3 settimane dall’inizio della terapia farmacologica, i monitoraggi successivi, andranno effettuati ogni 2-3 settimane qualora venisse modificato il dosaggio dei farmaci fino al raggiungimento dell’eutiroidismo (normali livelli di ormone tiroideo). I pazienti stabili, senza patologie concomitanti devono essere rivalutati dopo 3 mesi dall’inizio della terapia e poi ogni 6 mesi. Durante i controlli il veterinario potrà anche richiedere il monitoraggio della pressione sistemica che può aumentare nel corso del tempo nei gatti trattati (incidenza del 23%). In caso di insorgenza di ipertensione è bene venga trattata con terapia specifica. In seguito alla normalizzazione del T4 è possibile che vengano smascherate sottostanti alterazioni della funzionalità renale, con conseguente sviluppo di iperazotemia, infatti la malattia renale cronica e l’ipertiroidismo sono due problematiche che si incontrano spesso contemporaneamente nei pazienti anziani.La patologia renale cronica può essere evidente già alla diagnosi o svilupparsi (o risultare evidente) soltanto durante la terapia per l’ipertiroidismo. Nei gatti con concomitante malattia renale già evidente al momento della diagnosi di ipertiroidismo, il trattamento dell’ipertiroidismo è solitamente indicato, tuttavia con particolari attenzioni, in questi casi le aspettative di vita possono essere minori. Terapia alimentare: anche la dieta può essere di aiuto La sintesi degli ormoni tiroidei necessita di un sufficiente apporto di iodio alimentare.Una possibilità per trattare l'ipertiroidismo consiste pertanto nel ridurre le concentrazioni di ormoni tiroidei mediante la somministrazione di un alimento molto specifico a basso contenuto di iodio. Terapia chirurgica L’asportazione chirurgica della tiroide costituisce una valida possibilità terapeutica per l’ipertiroidismo. È una procedura efficace, rapida e di relativamente facile esecuzione. Nel 70% dei casi il coinvolgimento di entrambi i lobi tiroidei rende necessario l’esecuzione di una tiroidectomia bilaterale. Prima di eseguire l’intervento chirurgico è importante effettuare un periodo di terapia con farmaci antitiroidei per almeno due settimane per stabilizzare i livelli di T4 e fare si che il paziente risulti più stabile da un punto di vista cardiocircolatorio. Terapia con iodio radioattivo La terapia con iodio radioattivo è considerata d’elezione per l’ipertiroidismo felino; ciò è legato all’elevata efficacia terapeutica e la relativa assenza di complicazioni; risulta inoltre un’ottima opzione terapeutica nei casi di carcinoma tiroideo. A causa del potenziale radioattivo della molecola il trattamento può essere eseguito solo in strutture autorizzate, motivo per cui ad oggi il suo impiego è limitato a pochi centri. Aspettativa di vita La sopravvivenza media per gatti ipertiroidei senza una concomitante malattia renale cronica supera i 5,3 anni mentre se non trattata è una patologia progressiva con elevata morbidità e mortalità. La prognosi peggiora per i gatti ipertiroidei con carcinoma. Tuttavia, con un adeguato trattamento, anche questi pazienti possono vivere a lungo e morire per patologie non correlate alla neoplasia. Punti chiave L'ipertiroidismo è causato dall'aumento di produzione di ormoni tiroidei La patologia raramente e causata da una neoplasia maligna. L'eccesso di ormoni tiroidei può causare ipertensione, patologia renale, patologia cardiaca. I sintomi clinici più frequenti sono: dimagrimento, polifagia, vomito, iper-reattività, poliuria e polidipsia La diagnosi prevede l'esecuzione di esami ematologici e biochimici (allo scopo di escludere patologie concomitanti), esame delle urine, valutazione della funzione tiridea. Ulteriori esami utili sono l'ecocardiografia, radiografia, scintigrafia Le opzioni terapeutiche dell'ipertiroidismo felino possono essere farmacologiche, dietetiche, radioterapiche, chirurgiche. Dopo l'inizio della terapia farmacologica sono necessari controlli successivi dopo 2-3 settimane fino a raggiungimento dell'eutiroidismo, successivamente dopo 3 e 6 mesi. La sopravvivenza media per gatti ipertiroidei, in assenza di malattia renale cronica e senza diagnosi di carcinoma, a cui viene fatta terapia è di 5,3 anni. “DVM, Diplomato ECVIM-CA, EBVS® - European Veterinary Specialist in Small Animal Internal Medicine - Animali da compagnia, Endocrinologia non riproduttiva, medicina interna e terapia (Malattie Metaboliche).”Prof. Federico FracassiAutore #sppb-addon-1719818877863 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877863 img{}#sppb-addon-1719818877864 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877864 img{}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}
La pubblicità ci mostra mariti timidi che trovano mille scuse per non ammettere che con l’età la loro prostata inizia a causar loro qualche fastidio. Quello che la pubblicità non ci dice è che anche il nostro cane, come il suo padrone, può avere gli stessi disturbi. La prostata è la ghiandola che produce la parte liquida del seme e viene nutrita dall’ormone testosterone o meglio dalla sua forma attiva il Di-IdroTestosterone; con gli anni però la prostata va incontro ad un aumento di volume progressivo dipendente proprio dal testosterone e si evidenzia quindi l’alterazione nota come "iperplasia prostatica benigna". Come nell’uomo, l’aumento di volume della prostata provoca una compressione sugli organi vicini e da questa compressione derivano i sintomi che vedremo nel nostro cane. A differenza dell’uomo in cui l’aumento di volume della ghiandola avviene prevalentemente in senso concentrico, andando quindi a comprimere il collo della vescica (e il signore si dovrà alzare più volte durante la notte per urinare ... ma dirà di aver dimenticato la luce accesa), l’aumento della prostata nel cane avviene prevalentemente in senso eccentrico e quindi andrà in primo luogo a comprimere il retto. Uno dei primi sintomi quindi che di solito mostra il nostro cane affetto da "iperplasia prostatica benigna" è l’emissione di feci piatte oppure la difficoltà a defecare.L’altro sintomo molto precoce che si osserva in corso di "iperplasia prostatica benigna" è l’ipofertilità. Poiché con l’aumento di volume della prostata i suoi dotti interni possono restare occlusi, spesso in una prostata in iperplasia si ritroveranno anche delle cisti. Se le cisti diventano voluminose (a volte in realtà bastano anche pochi millimetri di diametro), le loro pareti si stirano e quindi iniziano a sanguinare.Ecco che compare l’altro sintomo frequente dell’iperplasia prostatica: il sanguinamento dal pene soprattutto dopo l’urinazione. Con l’evolversi della patologia i sintomi del nostro cane possono peggiorare e diventare importanti: difficoltà a deambulare, difficoltà a urinare, disoressia (alterazione dell’appetito) e abbattimento. In alcuni casi all’iperplasia prostatica benigna si può associare la prostatite sia acuta che cronica.Nel caso di prostatite cronica i sintomi sono quasi assenti mentre se il cane va incontro a prostatite acuta, la sintomatologia è imponente e la situazione diventa di emergenza. - Il cane avrà moltissimo dolore, farà fatica a camminare, spesso è presente febbre alta con nausea e forte abbattimento: è necessario correre subito dal Veterinario !!! Ma cosa possiamo fare per trattare l’iperplasia prostatica benigna e ancor meglio per prevenirla? A oggi sappiamo che più dell’80% dei cani maschi interi con età superiore ai 5 anni ne sono colpiti e che in realtà la condizione inizia a presentarsi verso il 40% dell’aspettativa di vita del cane. E’ importante quindi fare controlli regolari per iniziare le terapie appena è necessario. Oggi è disponibile un esame ematologico specifico (il CPSE) che ci indica se la prostata sta avendo dei problemi. Nel caso ce ne fosse indicazione a questo punto si esegue un’ecografia prostatica che valuta la prostata nel suo complesso: volume, aspetto, posizione e flussi sanguigni e che sarà in grado di dare tutte le indicazioni sullo stato di salute della ghiandola. E’ quindi fortemente consigliato chiedere al proprio Veterinario di fiducia di eseguire questo test almeno 1 volta l’anno a partire dai 4 anni di età e sarà poi lui a indicare se sono necessari ulteriori approfondimenti. Per la terapia sino a qualche anno fa la soluzione migliore per l’iperplasia prostatica era la sterilizzazione (castrazione) del cane: asportando i testicoli cessa la produzione di testosterone e quindi la prostata regredisce. Oggi fortunatamente ci sono terapie mediche efficacissime e anche molto semplici da somministrare per cui senza chirurgia il nostro cane potrà riavere una prostata normale. Nel caso in cui all’iperplasia si associ anche una prostatite cronica il Veterinario imposterà una terapia corretta anche a base di antibiotici, eventuali antinfimmatori e integratori per curare entrambe le patologie… e il proprietario potrà dormire sonni tranquilli !“DVM, Diplomata ECAR, EBVS ® - European Veterinary Specialist in Animal Reproduction (Fisiologia e patologia della Riproduzione, Ginecologia e Andrologia del cane, del gatto e dei mammiferi non convenzionali, Neonatologia)”Dr.ssa Maria Carmela PisuAutore #sppb-addon-1719818877863 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877863 img{}#sppb-addon-1719818877864 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877864 img{}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}

Le Ghiandole Epatoidi sono ghiandole sebacee modificate (senza sbocco) presenti nel cane e non nel gatto che circondano tutto l’ano (da cui anche il nome di ghiandole circumanali o perianali).Il termine “epatoide” deriva dal fatto che le loro cellule assomigliano a quelle del fegato. Tali ghiandole non sono da confondere con i sacchi anali o seni paranali, presenti alle ore “4” e “8” della circonferenza anale. Ghiandole Epatoidi sono anche presenti sul dorso della coda (dove costituiscono la così detta “ghiandola della coda”) e non è raro poterla osservare come area rilevata e spesso senza pelo, nei cani maschi anziani. Inoltre tali Ghiandole possono essere presenti occasionalmente, sulla groppa e sulla cute del prepuzio. Gli ormoni sessuali maschili hanno un effetto proliferativo su tali ghiandole, quelli femminili, al contrario, un effetto inibitorio. In caso di tumore benigno delle ghiandole epatoidi, non è rara la coesistenza di un tumore testicolare, soprattutto interstizioma (dalle cellule del Leydig o ghiandola interstiziale del testicolo, più spesso a comportamento benigno). Quali sono i tumori più frequenti delle ghiandole epatoidi? Nel cane maschio intero (non castrato), è l’adenoma/epitelioma epatoide ad essere rilevato più frequentemente (fino all’ 85-90% dei casi). I cani colpiti sono più spesso di piccola taglia, ma tutti i cani maschi anziani interi ne possono essere colpiti. Questo tumore si può presentare in molti modi: come nodulo singolo o multiplo rilevato e localizzato in un qualsiasi punto della circonferenza anale o anche alla sua immediata periferia, ricoperto da cute o ulcerato (a quel punto sanguinante, e per questo il cane è condotto a visita), o anche come ispessimento generalizzato di tutta la circonferenza anale. Possono coesistere noduli anche in altre sedi (coda, prepuzio o groppa) e, come già accennato, può rilevarsi anche un tumore testicolare. Il cane non manifesta particolari segni clinici, se non lambimento della parte, specie se ulcerato. All’esplorazione rettale non si evidenzia stenosi e l’animale non manifesta problemi particolari nel defecare. L’esame citologico da ago-aspirato consente di definire l’origine epatoide della lesione, mentre è più difficile la distinzione con un processo maligno ovvero l’adenocarcinoma epatoide. Quest’ultima è una neoplasia rara e solo raramente metastatica, che se localizzata intorno all’ano, provoca spesso stenosi anale, manifestata dal paziente con una più o meno grave difficoltà nel defecare. La diagnosi definitiva si effettua mediante biopsia ed esame istologico. Il trattamento chirurgico dell’adenoma/epitelioma, viene fatto precedere da esame radiografico del torace ed ecografico dell’addome e dei testicoli, e consiste nell’escissione “marginale” del/i nodulo/i e nella castrazione del soggetto. Vista l’ormodipendenza dei tumori benigni epatoidi, già la sola castrazione esita nella riduzione di almeno il 50% delle dimensioni dei noduli e, se ulcerati, nella risoluzione delle ulcere. In seguito all’asportazione chirurgica delle neoformazioni perianali delle Ghiandole Epatoidi, generalmente non si verifica incontinenza fecale in quanto, essendo le ghiandole epatoidi disseminate nel sottocute perianale e quindi in posizione esterna rispetto al muscolo sfintere esterno dell’ano, il muscolo stesso non è coinvolto nell’escissione. Dopo la chirurgia, noduli e testicoli devono essere sottoposti ad esame istologico. La ricomparsa di noduli in cani maschi castrati può essere interpretata come recidiva di un adenoma benigno (evento raro) o come sviluppo di malignità epatoide (adenocarcinoma, non più ormono-dipendente). L’adenoma/epitelioma epatoide può anche svilupparsi nelle femmine, in genere sterilizzate; in tal caso, l’origine degli ormoni è probabilmente surrenalica ed è opportuno indagare per eventuali patologie di queste ghiandole (ad es. sindrome di Cushing). L’adenocarcinoma delle ghiandole epatoidi è invece una forma maligna che se diagnosticata nella regione perianale, richiede chirurgie più aggressive che possono esitare in incontinenza fecale, specie se più di metà dell’anello anale deve essere completamente rimosso. Le eventuali (ma rare) metastasi ai linfonodi regionali sono contestualmente rimosse. La sopravvivenza dei cani affetti da questa forma maligna può essere soddisfacente.“DVM, Prof. Ordinario Clinica Chirurgica Veterinaria, Diplomato ECVS, EBVS® - European Specialist in Small Animal Surgery - (Oncologia Clinica, Chirurgia Oncologica, Chirurgia dei Tessuti Molli)”Prof. Paolo BuraccoAutore #sppb-addon-1719818877863 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877863 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877863 img{}#sppb-addon-1719818877864 { box-shadow: 0 0 0 0 #ffffff; margin:0px 0px 30px 0px;} @media (min-width: 768px) and (max-width: 991px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 20px;margin-left: 0px;}}@media (max-width: 767px) {#sppb-addon-1719818877864 {margin-top: 0px;margin-right: 0px;margin-bottom: 10px;margin-left: 0px;}}#sppb-addon-1719818877864 img{}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}.sp-page-builder .page-content #section-id-1719818877856{padding-top:30px;padding-right:0px;padding-bottom:30px;padding-left:0px;margin-top:0px;margin-right:0px;margin-bottom:0px;margin-left:0px;}#column-id-1719818877862{box-shadow:0 0 0 0 #fff;}

L’ipoadrenocorticismo o morbo di Addison è una sindrome conseguente ad una insufficiente produzione di ormoni glucocorticoidi e/o mineralcorticoidi da parte delle ghiandole surrenali. Queste due categorie di ormoni sono indispensabili per l’organismo. Le surrenali sono due piccole ghiandole poste in prossimità dei reni la cui importanza iniziò ad essere compresa solo verso la metà dell’800, quando il Dottor Thomas Addison descrisse, per la prima volta nell’uomo, una sindrome clinica associata ad una loro disfunzione (Addison, 1855). In suo onore a questa sindrome venne dato il nome di Morbo di Addison. La prima segnalazione di una forma di insufficienza surrenalica spontanea nel cane, quale entità clinica a sé stante, risale al 1953. Nell’uomo questa patologia ha una bassa incidenza (1 caso su 100.000 individui nei Paesi sviluppati, pari allo 0,001%); nel cane l’ipoadrenocorticismo è raro, ma la prevalenza si aggira approssimativamente tra lo 0,06% e lo 0,28%. Un recente studio ha individuato una incidenza di 2,3 casi ogni 10000 soggetti.Fisiologia:Le ghiandole surrenali si compongono di una porzione più interna, detta midollare, che secerne catecolamine e di una porzione più esterna, detta corticale. Quest’ultima è a sua volta suddivisa, da un punto di vista istopatologico, in tre strati che procedendo dall’esterno verso l’interno sono: la zona glomerulosa responsabile della produzione di mineralcorticoidi (aldosterone), la zona fascicolata deputata alla sintesi di glucocorticoidi (cortisolo) e la zona reticolare nella quale vengono prodotti androgeni (Figura 2).La sintesi e secrezione di cortisolo, più importante esponente dei glucocorticoidi, è regolata dall’asse ipotalamo-ipofisi-surrene tramite i classici meccanismi di feedback positivo e negativo.I glucocorticoidi svolgono un ruolo di vitale importanza nel mantenere una normale omeostasi. Oltre a contrastare gli effetti dello stress, il cortisolo esalta gli effetti delle catecolamine sui vasi, mantiene una normale pressione sanguigna, stimola la gluconeogenesi epatica e il catabolismo di proteine e grassi, garantisce una corretta funzionalità e integrità della mucosa gastrointestinale.La carenza di questo ormone comporta quindi una maggiore sensibilità allo stress, l’incapacità di mantenere il tono vasale, l’integrità endoteliale e la conseguente ipotensione, ipoglicemia e debolezza muscolare, sintomi gastroenterici quali disoressia/anoressia, vomito e diarrea. La sintesi e secrezione di aldosterone, principale rappresentante dei mineralcorticoidi, è regolata dall’asse renina-angiotensina, dalla concentrazione plasmatica di potassio e, per una quota quasi trascurabile, dalla concentrazione di ACTH.Aumentando l’assorbimento di sodio (e indirettamente di acqua) e la secrezione di potassio e ioni idrogeno a livello renale e in altri siti meno rilevanti, l’aldosterone svolge un ruolo fondamentale nel garantire l’equilibrio salino dell’organismo e ne condiziona in parte anche il pH.Pertanto, una carenza di tale ormone comporta lo svilupparsi di alterazioni elettrolitiche (iponatremia, ipocloremia, iperkaliemia e acidosi metabolica). Le perdite idriche conseguenti alla mancata capacità di trattenere sodio e cloro comportano una riduzione del fluido extracellulare che, nel tempo, esitano inevitabilmente in una condizione di ipovolemia, ipotensione, riduzione della gittata cardiaca, riduzione della filtrazione glomerulare e iperazotemia prerenale. Classificazione: L’ipoadrenocorticismo o Morbo di Adddison si classifica in una forma primaria e una forma secondaria . L’ipoadrenocorticismo primario, più frequente (circa il 95% dei casi), è causato da una distruzione di entrambe le ghiandole surrenali conseguente, quasi sempre, ad un meccanismo autoimmune, e si rende clinicamente manifesta solo quando è interessato più del 90% della corteccia surrenalica.Altre possibili cause di distruzione della corteccia surrenalica, sebbene più insolite, sono alcune patologie granulomatose specifiche (quali l’istoplasmosi e la blastomicosi), l’amiloidosi, lesioni ischemiche da infarti emorragici locali (secondari a traumatismi a coagulopatie o a tossicosi da anticoagulanti cumarinici) o anche neoplasie metastatiche (carcinomi polmonari, mammari, prostatici, gastrici e pancreatici, o melanomi).L’ipocortisolismo primario può infine verificarsi anche per cause iatrogene conseguenti ad eccessiva somministrazione di farmaci, quali mitotane e trilostano, utilizzati per il trattamento dell’ipercortisolismo. Una predisposizione genetica-ereditaria all’ipoadrenocorticismo primario legata ad un gene autosomico recessivo è stata individuata in razze quali Barbone, cane d’acqua Portoghese, Nova Scotia Duck Tolling Retriever e Bearded Collie. Ad eccezione di queste razze, nella popolazione generale è stata individuata una predisposizione per il sesso femminile (circa del 70%) e una probabilità 3 volte maggiore per i soggetti sterilizzati (sia maschi che femmine) rispetto ai soggetti interi di contrarre la malattia.Sono interessati soprattutto soggetti giovani e di mezza età con una età mediana di 4 anni (da 4 mesi a 14 anni) (Peterson et al, 1996). L’ipoadrenocorticismo secondario, invece, è causato da una ridotta secrezione dell’ormone trofico specifico (ormone adrenocorticotropo o ACTH) da parte dell’ipofisi.Nel cane, come nell’uomo, questa condizione è generalmente conseguente a processi neoplastici, meno comunemente a problemi infiammatori o traumatici.Il mancato stimolo da parte dell’ACTH determina l’atrofia della zona fascicolata e, conseguentemente, una carenza glucocorticoidea. Molto importante da un punto di vista clinico è l’insufficienza surrenalica secondaria iatrogena conseguente alla somministrazione di corticosteroidi. Tale fenomeno è di comune riscontro nel cane, anche se raramente comporta una sintomatologia clinica evidente.Il trattamento protratto con farmaci corticosteroidi inibisce l’asse ipotalamo-ipofisario e può quindi comportare atrofia surrenalica secondaria.La sensibilità individuale ai corticosteroidi è molto variabile: in alcuni individui l’atrofia della corticale si instaura dopo pochi giorni di somministrazione, in altri individui questo non accade. La soppressione dell’asse ipotalamo-ipofisario-corticosurrenalico può persistere per settimane o mesi dopo la sospensione dei glucocorticoidi, a seconda della dose, della preparazione, della durata del trattamento e della sensibilità individuale. Solitamente l’insufficienza surrenalica iatrogena si verifica in seguito a terapie croniche; è stata documentata non solo con glucocorticoidi iniettabili od orali, ma anche con farmaci ad uso topico dermatologico, oftalmico ed auricolare. Pertanto, l’effettuazione di test di funzionalità surrenalica in soggetti sottoposti a terapie corticosteroidee deve essere posticipata da un minimo di 48 ore (nel caso di una singola somministrazione di prednisone o prednisolone) fino a 6-8 settimane dalla sospensione del farmaco (nel caso di forme deposito) per poter garantire una interpretazione corretta dei risultati . Come già detto, la carenza di ACTH che caratterizza la forma secondaria (anche quella iatrogena) determina l’atrofia della zona fascicolata ma non della zona glomerulosa, dal momento che l’attività secretoria di quest’ultima è condizionata solo in misura trascurabile dall’ACTH.Per questo motivo la forma secondaria è caratterizzata dalla sola carenza glucocorticoidea, mentre la forma primaria si associa generalmente a carenza sia glucocorticoidea che mineralcorticoidea.Tuttavia, oltre un 30% dei casi di ipoadrenocorticismo primario presenta, al momento della diagnosi, concentrazioni elettrolitiche normali; tali casi potrebbero essere confusi con forme secondarie. Questa condizione, più insidiosa da diagnosticare, è stata definita “atipica”.La discriminante in questo caso è rappresentata dalla concentrazione di ACTH endogeno che risulta bassa nel caso della forma secondaria, mentre è elevata nella forma primaria. Possibili ipotesi che giustifichino l’assenza di alterazioni elettrolitiche sono: un coinvolgimento più tardivo della zona glomerulosa, l’influenza di malattie concomitanti (es. ipotiroidismo) oppure altri fattori, diversi dall’aldosterone, implicati nel mantenere l’equilibrio elettrolitico. Nel cane l’ipoadrenocorticismo è una patologia piuttosto rara, un recente studio del 2016 ha individuato una incidenza di 2,3 casi ogni 10000 soggetti. Una predisposizione genetica-ereditaria all’ipoadrenocorticismo primario legata ad un gene autosomico recessivo è stata individuata in razze quali Barbone, cane d’acqua Portoghese, Nova Scotia Duck Tolling Retriever e Bearded Collie. Ad eccezione di queste razze, per le quali non è stata dimostrata una predisposizione di sesso, nella popolazione generale è stata individuata una predisposizione per il sesso femminile (circa del 70%) e una probabilità 3 volte maggiore per i soggetti sterilizzati (sia maschi che femmine) rispetto ai soggetti interi di contrarre la malattia. Sono interessati soprattutto soggetti giovani e di mezza età con una età mediana di 4 anni (da 4 mesi a 14 anni).Sintomatologia:I segni clinici in corso di Ipoadrenocorticismo ipofisario o Morbo di Addison canino possono comparire in maniera acuta o stabilirsi in modo graduale, in quest’ultimo caso caratterizzati da un andamento “altalenante” (sintomi che “vanno e vengono”), e la cosiddetta crisi addisoniana è in genere scatenata da un evento stressante. I sintomi più frequentemente individuati dai proprietari di cani affetti da insufficienza surrenalica sono quelli secondari alla carenza glucocorticoidea: anoressia/disoressia, vomito, letargia/depressione, debolezza/astenia, dimagramento, diarrea e tremori; più raramente anche poliuria, polidipsia e dolore addominale. Quando è presente anche carenza mineralcorticoidea, i sintomi clinici tendono ad essere più gravi e caratterizzati da poliuria/polidipsia più intensa, grave disidratazione fino al collasso e shock ipovolemico. Meno comunemente si possono osservare crisi convulsive ipoglicemiche, crampi muscolari e sanguinamenti gastroenterici. Preoccupazione dei proprietari Peterson e coll. (1996) Feldman e Nelson (2004) Anoressia 91,6% 88% Letargia 93,8% 85% Dimagramento 48% 82% Vomito 76,4% 68% Debolezza/astenia 51% Diarrea 41,3% 35% Sintomi “altalenanti” 43,1% 25% Tremori 27,1% 17% Poliuria/polidipsia 24% 17% Collasso 10% Addome dolente 8% Come i sintomi, anche i reperti clinici sono estremamente vaghi e aspecifici, facilmente confondibili con patologie renali, gastrointestinali, neuromuscolari ed infettive (patologie tra l’altro molto più frequenti negli animali d’affezione rispetto al morbo di Addison). Le alterazioni che il veterinario potrà rilavare durante la visita clinica sono: condizioni generali scadenti, letargia, debolezza, grave disidratazione, dolore addominale, bradicardia, polso debole, ipotermia, ridotto tempo di riempimento capillare e altri segni di shock ipovolemico (la maggior parte dei pazienti presentano una bassa pressione sistolica). Sintomi Clinici alla visita Peterson e coll. (1996) Feldman e Nelson (2004) Letargia/depressione 86,2% 87% Dimagramento 82% Debolezza/astenia 76,4% 66% Disidratazione 46,2% 41% Collasso 34,7% 24% Polso debole 34,7% 22% Bradicardia 22% Prolungamento TRC 34,7% Melena/ematochezia 15,1% 17% Ipotermia 33,8% 15% Addome dolente 7% Diagnosi:Per giungere alla diagnosi di questa patologia piuttosto rara, il veterinario, a seconda della presentazione del paziente e della successiva visita clinica, potrà richiedere alcuni esami sia di laboratorio che strumentali (Emogramma, Profilo biochimico, Ecografia addominale, RX toracico , Elettrocardiogramma). Ciascuno di questi esami diagnostici potrà fornire importanti informazioni che aiutano ad individuare la patologia. Emocromocitometrico: Le alterazioni più comunemente riscontrate all’esame emocromocitometrico sono rappresentate da un lieve stato di anemia normocitica normocromica non rigenerativa e, decisamente più caratteristico, da un quadro di linfocitosi ed eosinofilia. Profilo biochimico: Per quanto riguarda le altre alterazioni al profilo biochimico, quelle senza dubbio più frequenti sono quelle relative alla funzionalità renale. L’incremento di urea e creatinina è dovuto solitamente ad una grave insufficienza “prerenale” conseguente allo stato di ipovolemia, ipotensione e ridotta perfusione renale. Peterson e coll. (1996) Melian e Peterson (1996) Feldman e Nelson (2004) Ipercalcemia 30,7% 19,1% 29% Ipoglicemia 16,7% 35% 22,9% Ipoprotidemia 12,5% 23,8% 14% Ipoalbuminemia 6,3% 12,2% 18% Iperazotemia 88,4% 76,2% 88,5% Aumento della creatininemia 65,6% 59,5% 61% PS urinario

